Organisation et gestion des laboratoires
Topic outline
-
Ce cours est destiné aux étudiants de licence 3 en microbiologie, biotechnologie et biochimie Il couvre l'intégralité du programme de la matière « Organisation et gestion des laboratoires » dispensée au semestre VI du centre universitaire Nour Bachir – El-Bayadh.
La maîtrise de l'organisation et de la gestion des laboratoires est une compétence fondamentale pour tout professionnel des sciences de la nature et de la vie (SNV). Elle conditionne la qualité des résultats analytiques, la sécurité des personnels et la conformité aux normes nationales et internationales (ISO, OMS, ALGERAC).
-
Forum
-
-
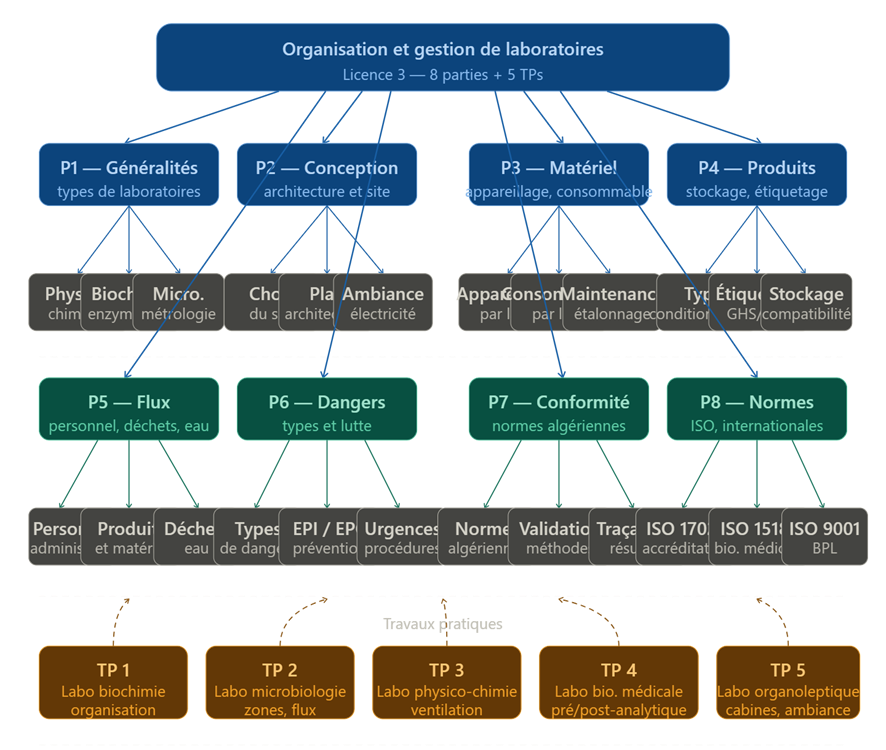
Le cours "Organisation et gestion de laboratoires, L3" comporte 8 parties (sections) :
La première partie :
– Généralités.
– Types de laboratoires : physicochimique, biochimie, enzymologie/enzymeologie appliquée, microbiologie, organoleptique, métrologie, biologie médicale, autres types de laboratoires.
La seconde partie :
– Conception des laboratoires.
– Choix du site.
– Plan architectural : superficie, plan de répartition des salles, conception des sols, conception des murs (isolation), conception des paillasses, conditionnement électrique, conditions d’ambiance.
La troisième partie :
– Matériel : appareillage pour chaque type de laboratoire, consommable pour chaque type de laboratoire.
La quatrième partie :
– Produits de laboratoire : type de produits, conditionnement, étiquetages, endroit de stockage.
La cinquième partie :
– Gestion des flux : responsables administratifs, gestion du personnel, gestion des produits et du matériel, gestion des déchets, gestion de l’eau.
La sixième partie :
– Dangers pouvant être rencontrés dans un laboratoire : types de dangers, moyens de lutte.
La septième partie :
– Conformité des analyses aux normes algériennes et internationales.
La huitième partie :
– Normes internationales en vigueur d’organisation des laboratoires
Travaux pratiques :
TP1 – Organisation d’un laboratoire type de biochimie.
TP2 – Organisation d’un laboratoire type de microbiologie.
TP3 – Organisation d’un laboratoire type de Physico-Chimie.
TP4 – Organisation d’un laboratoire type de biologie médicale.
TP5 – Organisation d’un laboratoire type d’analyses organoleptiques.
-
Dr. NAIMI Mostefa
Maître de conférences A
Département des Sciences Biologiques, bureau N°1
 m.naimi@cu-elbayadh.dz mostecoc@yahoo.fr mosttus@yahoo.fr
m.naimi@cu-elbayadh.dz mostecoc@yahoo.fr mosttus@yahoo.fr  https://www.researchgate.net/profile/Naimi_Mostefa
https://www.researchgate.net/profile/Naimi_Mostefa https://scholar.google.com/citations?hl=en&user=YG58ihMAAAAJ
https://scholar.google.com/citations?hl=en&user=YG58ihMAAAAJ https://www.facebook.com/mostecoc
https://www.facebook.com/mostecoc -
– Chargé du cours & TP : Dr. NAIMI Mostefa.
– Intitulé de l’UE : Biosécurité.
– Intitulé de la matière : Organisation & Gestion des Laboratoires (OGL).
_ Licence : Microbiologie, Biotechnologie & Biochimie.
– UE : Découverte.
– Coefficient : 2.
– Crédits : 3.
Volume horaire :
– Séance du cours (1 h 30).
– Séance TP (1 h 30).
Modalité d'évaluation :
– Examen écrit : 60 %.
– Évaluation continue : 40 % (note TD : 20 %, note TP : 20 %).
-
À la fin du semestre, l'étudiant sera capable de :
– Décrire les différents types de laboratoires liés aux sciences biologiques et leurs missions spécifiques.
– Appliquer les principes généraux de conception architecturale d'un laboratoire conforme aux normes.
– Identifier et sélectionner le matériel (appareillage et consommables) adapté à chaque type de laboratoire.
– Gérer les produits de laboratoire : stockage, étiquetage, compatibilité chimique et sécurité.
– Décrire les qualifications requises pour chaque fonction du personnel de laboratoire.
– Identifier les risques (physiques, biologiques, chimiques) et appliquer les mesures de prévention.
– Référencer les normes algériennes et internationales applicables aux laboratoires.
-
En ligne/hybride
Centré sur le travail personnel (questions, participation et prise de parole; exposés),
Afin de mieux se préparer à l'interrogation de TP et à l’examen.
Contrôle continu et examen.
Support de cours & Modalités d'évaluation
Support de cours
Fiche de consignes de rédaction de l’exposé
Lignes de conduite
Horaire et lieu (cours).
Respect.
Présence obligatoire.
Lectures complémentaires
Les ressources en ligne sont extrêmement nombreuses (sur Google par exemple, tapez « mot clé » et sélectionnez les sites les plus rigoureux).

-
La maîtrise des différentes matières de biologie, principalement : microbiologie, chimie, biochimie et enzymologie. Ces connaissances constituent le socle disciplinaire indispensable avant d'aborder le cours. Elles correspondent aux acquis attendus de licence 1 et de licence 2 en sciences biologiques.
Matière source
Connaissances requises
Niveau de maîtrise attendu
Chimie générale (L1)
Nomenclature des composés inorganiques et organiques ; états de la matière ; loi de Beer-Lambert ; solutions et concentrations.
Calculer une concentration massique et molaire ; préparer une solution de titre connu.
Biochimie (L2)
Structures des glucides, lipides, protéines et acides nucléiques ; métabolisme énergétique de base.
Identifier les principales familles de biomolécules et leur rôle fonctionnel.
Microbiologie générale (L2)
Classification des microorganismes (bactéries, levures, moisissures, virus) ; structure cellulaire procaryote vs eucaryote ; notions de culture microbienne.
Nommer les principaux groupes microbiens ; décrire le cycle de croissance bactérienne.
Physique (L1)
Unités SI ; principes des mesures physiques (masse, volume, température, pH, absorbance) ; erreurs et incertitudes.
Appliquer les unités SI ; identifier les sources d'erreur dans une mesure.
Notions de base sur les risques biologiques, chimiques et physiques en laboratoire.
Identifier un pictogramme de danger ; appliquer les règles de base de sécurité.
Enzymologie (L2)
Notion d'enzyme, de substrat, de réaction enzymatique ; cinétique de Michaelis-Menten.
Décrire le rôle d'une enzyme dans une réaction biochimique.
-
Opened: Saturday, 4 April 2026, 10:54 AMCloses: Thursday, 9 April 2026, 10:54 AM
-
-
République Algérienne Démocratique et Populaire
Ministère de l'Enseignement Supérieur et de la Recherche Scientifique
Centre Universitaire Nour Bachir – El-Bayadh
Département des Sciences Biologiques
Organisation & Gestion des Laboratoires
Licence 3 – Microbiologie, Biotechnologie & Biochimie | Semestre VI
PARTIE 1 — Généralités
Définition du laboratoire, composantes, types de laboratoires
Dr. NAIMI Mostefa
Maître de Conférences A – Département des Sciences Biologiques
Année universitaire 2025–2026
Partie 1 — Généralités
1.1 Définition d'un laboratoire
Le terme « laboratoire » vient du latin laboratorium, dérivé de laborare (travailler). Il désigne un espace dédié à l'exécution d'activités scientifiques contrôlées : recherches, analyses, tests, mesures et expérimentations.
Un laboratoire rassemble de façon organisée :
• Les moyens humains : personnel technique (techniciens, ingénieurs, biologistes), personnel administratif et personnel de soutien ;
• Les moyens matériels : installations, mobilier et équipements.
Définition officielle
Un laboratoire est un espace structuré rassemblant des ressources humaines qualifiées et des ressources matérielles adaptées, dans le but d'exécuter des activités d'analyse, de recherche, d'essai ou d'étalonnage, selon des méthodes validées et des procédures documentées.

Figure N°1.1 : Infrastructures et postes de travail du laboratoire.
1.2 Composantes d'un laboratoire type
1.2.1 Les installations
En plus du local aménagé, les installations comprennent principalement les paillasses (plans de travail). On distingue :
• Paillasses construites en dur (fixes) ou amovibles (mobiles) ;
• Paillasses sèches (sans arrivée d'eau) ou humides (avec évier intégré) ;
• Paillasses avec ou sans dosseret (tablette arrière pour ranger le matériel).
La hauteur recommandée du plan de travail est comprise entre 720 mm et 900 mm (norme ergonomique).

Figure N°1.2 : Paillasses de manipulation avec dosseret et postes de travail.
1.2.2 Le mobilier
Le mobilier d'un laboratoire comprend l'ensemble des éléments non-techniques permettant d'organiser l'espace de travail :
• Armoires : métalliques, coffre-fort (produits dangereux), vitrées (réactifs courants) ;
• Tabourets et chaises de laboratoire ergonomiques ;
• Portemanteaux et vestiaires pour les équipements de protection individuelle (EPI) ;
• Bureaux pour la rédaction des rapports et la documentation.

Figure N°1.3 : Mobilier de bureau du laboratoire.
1.2.3 L’équipement
L'équipement de laboratoire est classé en deux catégories fondamentales : (1) le consommable et (2) le non consommable.
Tableau N°1.1 : Classification du matériel de laboratoire, durée de vie et maintenance.
Équipement Consommable
Matériel à usage unique ou à renouvellement fréquent :
– Verrerie : béchers, éprouvettes, fioles jaugées, erlenmeyers, pipettes graduées et de précision, pissettes, entonnoirs, réfrigérants, etc.
– Petits consommables : gants, bavettes, coiffes, embouts de micropipettes, tubes Eppendorf, filtres, etc.
– Réactifs et produits chimiques à usage unique ou de courte durée de vie.
Équipement non consommable
Matériel durable nécessitant entretien, étalonnage et maintenance :
– Appareils de mesure quantitative (analyse quantitative) : balances analytiques, centrifugeuses, pH-mètres, conductimètres, polarimètres, spectrophotomètres, photomètres de flamme, etc.
– Appareils d'analyse qualitative : systèmes de chromatographie (HPLC, CPG), électrophorèse, ELISA, etc.
– Appareils de conditionnement et de préparation : autoclaves, étuves, fours à moufle, bains-marie, distillateurs, etc.

Figure N°1.4 : L'équipement de laboratoire.
Tout équipement non consommable doit faire l'objet, de manière systématique et documentée, de :
1. Entretien préventif et correctif (vérification périodique du bon fonctionnement) ;
2. Étalonnage (calibrage) — vérification de la justesse des mesures par rapport à des étalons traçables ;
3. Maintenance — selon les instructions du fabricant et le plan de maintenance du laboratoire.
1.3 Types de laboratoires
Les laboratoires liés aux sciences biologiques et à leurs applications se déclinent en plusieurs types spécialisés, chacun répondant à des missions analytiques précises.
1.3.1 Laboratoire de Physicochimie
Ces laboratoires sont actifs dans les secteurs agroalimentaire et pharmaceutique (laboratoires de contrôle de qualité, de répression des fraudes, d'autocontrôle). Ils reçoivent des produits issus de la production alimentaire et/ou pharmaceutique et mesurent :
• Paramètres physiques : apparence, couleur, odeur, volume, triage, granulométrie ;
• Paramètres chimiques généraux : pH, conductivité, densité, température ;
• Composition : eau, matière sèche, protéines, matières grasses, glucides, cendres, matières minérales ;
• Composés spécifiques : nitrates, nitrites, phosphates, métaux lourds, pesticides, antibiotiques, arômes, vitamines, allergènes, conservateurs ;
• Indices analytiques : saponification, acide, iode, réfraction, acidité, stabilité.
1.3.2 Laboratoire de Biochimie
Ces laboratoires sont actifs dans le secteur médical (biochimie clinique) et dans le secteur alimentaire (biochimie alimentaire).
• Les laboratoires de biochimie clinique reçoivent des échantillons biologiques (sang, urines, LCR, etc.) et réalisent des dosages variés :
• Bilan lipidique : cholestérol total, triglycérides, LDL, HDL ;
• Bilan glucidique : glycémie à jeun, HbA1c, test d'hyperglycémie provoquée ;
• Bilan rénal : urée, créatinine, clairance de la créatinine ;
• Ionogramme : sodium, potassium, chlorures, bicarbonates ;
• Enzymes : ASAT, ALAT, GGT, phosphatases alcalines, amylase, lipase ;
• Gaz du sang : pression partielle d'oxygène (pO₂), pression partielle de CO₂ (pCO₂), pH.
1.3.3 Laboratoire d'Enzymologie et Enzymologie Appliquée
Ces laboratoires étudient les propriétés des enzymes (cinétique, inhibition, caractérisation biochimique) et leurs applications industrielles. Ils réalisent notamment :
• Purification et caractérisation d'enzymes à partir de sources biologiques ;
• Détermination des paramètres cinétiques (Km, Vmax, constante d'inhibition) ;
• Mise au point de dosages enzymatiques automatisés ;
• Optimisation de l'utilisation d'enzymes en industrie (agroalimentaire, pharmacie, détergents).
1.3.4 Laboratoire de Microbiologie
Ces laboratoires sont actifs dans le secteur médical (microbiologie clinique : bactériologie, virologie, parasitologie, mycologie) et dans le secteur alimentaire (microbiologie alimentaire : hygiène, contrôle qualité, répression des fraudes).
Les laboratoires de microbiologie médicale réalisent :
• Examens cytobactériologiques des urines (ECBU) ;
• Hémocultures et coprocultures ;
• Antibiogrammes (méthodes des disques selon le Comité de l'Antibiogramme) ;
• Tests d'efficacité de la conservation antimicrobienne.
Les laboratoires de microbiologie alimentaire réalisent :
• Dénombrement et identification des germes pathogènes (bactéries, levures, moisissures) selon les normes ISO et JORA ;
• Validation et vérification de méthodes microbiologiques ;
• Recherche de germes indicateurs d'hygiène et de germes pathogènes spécifiques.
1.3.5 Laboratoire Organoleptique
Ce type de laboratoire utilise les sens humains (analyse sensorielle) pour évaluer les caractéristiques organoleptiques des produits alimentaires. L'instrument de mesure est l'homme à travers ses 5 sens :
Tableau N°1.2 : Bases de l'analyse sensorielle, sens et paramètres.
Sens
Paramètre évalué
Exemples d'application
Vision
Couleur, forme, aspect, mouvement
Teinte d'un vin, texture d'un fromage, limpidité d'une huile
Odorat
Odeur et arôme
Fraîcheur du pain, arômes fruités, rancissement
Somesthésie
Toucher, texture, température
Onctuosité d'un yaourt, croquant d'une biscotte
Goût
Sucré, salé, acide, amer, umami
Équilibre gustatif d'un produit formulé
Audition
Sons émis lors de la mastication
Croquant, croustillant, pétillant
1.3.6 Laboratoire de Métrologie
Ces laboratoires exercent un ensemble d'opérations nécessaires pour s'assurer qu'un équipement de mesure répond aux exigences correspondant à l'utilisation prévue. Les activités comprennent :
• Vérification : contrôle de la conformité d'un instrument par rapport à des exigences réglementaires ;
• Étalonnage : établissement de la relation entre les valeurs indiquées par un instrument et les valeurs correspondantes des grandeurs mesurées, à l'aide d'étalons traçables ;
• Maintenance : ensemble des actions permettant de maintenir ou rétablir l'état de fonctionnement ;
• Réparation : remise en état après défaillance.
1.3.7 Laboratoire de Biologie Médicale
Ces laboratoires, présents dans les secteurs public et privé, intègrent plusieurs disciplines complémentaires :
• Biochimie clinique ;
• Microbiologie clinique (bactériologie, virologie, parasitologie, mycologie) ;
• Sérologie et immunologie (dosage d'immunoglobulines, dépistage HIV, hépatites, typage antigénique) ;
• Hématologie (morphologie, physiologie et numération des cellules sanguines) ;
• Anatomopathologie (ANAPATH) : biopsies, pièces opératoires, autopsies ;
• Pharmacotoxicologie : dosage de médicaments et de toxines diverses.
1.3.8 Autres types de laboratoires
D'autres laboratoires liés aux sciences de la nature et de la vie incluent :
• Laboratoires d'écologie et d'environnement ;
• Laboratoires de géologie et de minéralogie ;
• Laboratoires de zoologie et de botanique ;
• Laboratoires d'analyses vétérinaires ;
• Laboratoires de biologie moléculaire et de génomique ;
• Laboratoires de biotechnologies (fermentation industrielle, culture cellulaire...).
-
QuizOpened: Saturday, 4 April 2026, 11:07 AMCloses: Thursday, 9 April 2026, 11:07 AM
-
Partie 2— Conception des laboratoires : Choix du site, plan architectural, sols, murs, paillasses, électricité, ambiance.
République Algérienne Démocratique et Populaire
Ministère de l'Enseignement Supérieur et de la Recherche Scientifique
Centre Universitaire Nour Bachir – El-Bayadh
Département des Sciences Biologiques
Organisation & Gestion des Laboratoires
Licence 3 – Microbiologie, Biotechnologie & Biochimie | Semestre VI
PARTIE 2 — Conception des Laboratoires
Choix du site, plan architectural, sols, murs, paillasses, électricité, ambiance
Dr. NAIMI Mostefa
Maître de Conférences A – Département des Sciences Biologiques
Année universitaire 2025–2026
Partie 2 — Conception des laboratoires
2.1 Choix du site
Le choix de l'emplacement d'un laboratoire est une décision stratégique qui conditionne la sécurité, la qualité des analyses et le bien-être du personnel. Le laboratoire doit :
• Être installé loin des zones de vie (habitations, espaces de restauration, salles de réunion) ;
• Être effectivement séparé des secteurs siège d'activités incompatibles (stockage alimentaire, ateliers de production générant des vibrations ou des contaminants) ;
• Être implanté dans un environnement de travail calme, à l'abri des interruptions extérieures ;
• Disposer d'une bonne aération et d'une ventilation adaptée, réduisant la dissémination des agents microbiologiques et la contamination aéroportée (particulièrement critique en biologie moléculaire).
2.2 Plan architectural
2.2.1 Superficie
Le laboratoire doit avoir une surface suffisante pour maintenir les zones de travail en ordre et propres. La superficie doit être adaptée :
• Au volume et à la nature des analyses réalisées ;
• À l'organisation générale interne du laboratoire ;
• Au nombre de postes de travail et de personnels ;
• Aux exigences de sécurité (dégagements, voies d'évacuation, zones tampon).

Figure N°2.1 : Infrastructures et postes de travail du laboratoire.
2.2.2 Plan de répartition des salles — Laboratoire d'analyses médicales
Les salles d'un laboratoire d'analyses médicales doivent respecter une structure organisationnelle obligatoire permettant de manipuler, analyser et identifier toutes matières biologiques sans risque. Le laboratoire doit comprendre :
• Salle de prélèvement indépendante (avec accès direct depuis la zone d'accueil des patients) ;
• Zone de réception, de stockage et de préparation des échantillons et des aliquotes ;
• Zone de réalisation des analyses ;
• Salle indépendante pour la préparation et la stérilisation des milieux de culture et du matériel (si activité microbiologique) ;
• Salle indépendante de décontamination, de nettoyage des matériels (autoclave, four Pasteur) et laverie.

Figure N°2.2 : Plan d'aménagement d'un laboratoire en une seule salle (mono-salle).
2.2.3 Plan de répartition des salles — Laboratoires de Microbiologie et Biologie Moléculaire
L'organisation du circuit des échantillons biologiques doit prévenir toute contamination croisée inter-échantillons. Le plan doit respecter le principe fondamental de la « marche en avant » des échantillons biologiques.
Tableau N°2.1 : Principe de la marche en avant.
Principe de la marche en avant
Les échantillons biologiques circulent dans un sens unique, du plus propre vers le moins propre, sans jamais revenir en arrière. Ce principe, issu des normes d'hygiène alimentaire (ISO 22000), est transposé aux laboratoires de microbiologie pour prévenir les contaminations croisées entre échantillons et entre zones de travail.
Pour un laboratoire de microbiologie, les salles sont classées du plus propre au moins propre dans l'ordre suivant :
• Salle de stérilisation et/ou de désinfection (zone la plus propre) ;
• Salle de manipulation (clair, à l'abri des courants d'air) ;
• Salle annexe pour l'incubation ;
• Salle de décontamination ;
• Zone de stockage des milieux de culture, réactifs, souches de référence ;
• Zone de réception et de stockage des échantillons (zone la moins propre).
2.2.4 Conception des sols
Les sols des laboratoires doivent répondre aux exigences techniques suivantes :
• Résistants à l'usure mécanique, au poinçonnement et aux chocs ;
• Antidérapants (coefficient de frottement adapté au travail debout) ;
• Imperméables et résistants aux agents nettoyants, désinfectants et aux produits chimiques utilisés ;
• Conçus pour réduire la rétention de poussières (limitant les sources de contamination microbienne) ;
• Carrelage non recommandé en microbiologie (joints = source de contamination) ; préférer les revêtements sans joints (résines époxy, PVC homogène) ;
• Facilement accessibles pour permettre un nettoyage régulier et une décontamination efficace ;
• Remonter d'au moins 10 cm le long des murs avec une moulure concave (gorge) pour limiter l'accumulation de particules et faciliter la décontamination.

Figure N°2.3 : Laboratoire, moulure concave (gorge).

Figure N°2.4 : Laboratoire, revêtements sans joints (résines époxy).
2.2.5 Conception des murs (isolation)
Les murs des laboratoires doivent être :
• Lisses et faciles à nettoyer (surfaces non poreuses, sans relief) ;
• Résistants aux produits détergents et aux désinfectants utilisés dans les laboratoires ;
• Étanches, résistants aux produits de nettoyage et de désinfection ;
• Exempts de fissures ou craquelures pouvant constituer des sources de contamination microbienne ou chimique ;
• Conçus pour réduire la transmission de bruit et les vibrations (isolation phonique et mécanique).
2.2.6 Conception des paillasses
Les paillasses (plans de travail) sont l'élément central du laboratoire. Elles doivent répondre aux critères suivants :
• Revêtement lisse, résistant, imperméable, incombustible, facile à nettoyer et à désinfecter ;
• Caractéristiques anti-adhérence microbienne (surface non colonisable par les microorganismes) ;
• Ne pas sceller les paillasses au mur (mobilité pour les évolutions du laboratoire et accès aux canalisations) ;
• Limiter le nombre de pieds pour faciliter le nettoyage du sol en dessous ;
• Limiter le nombre de joints du revêtement de surface ;
• Hauteur du plan de travail recommandée : entre 720 mm et 900 mm (norme ergonomique).

Figure N°2.5 : Laboratoire, Matériaux des plans de paillasse.
Tableau N°2.2 : Comparaison des différents matériaux de revêtement pour paillasses de laboratoire : stratifié blanc, verre émaillé, résine compacte, Trespa® et grès étiré.
Matériau
Description
Applications Clés
Stratifié blanc
Bois hydrofuge avec revêtement stratifié de 1,2 mm. Épaisseur totale de 30 mm. Surface mate, lisse et antireflet.
Laboratoires de contrôle standard, physique et instrumentation. À proscrire pour les produits chimiques agressifs, la microbiologie ou la virologie.
Glace émaillée (Verre trempé)
Verre opalin de 6 mm sur support bois hydrofuge de 19 mm (25 mm au total). Idéal pour un nettoyage et une stérilisation facile.
Microbiologie, analyses médicales et tout environnement nécessitant une décontamination totale.
Résine compacte
Panneau de 8 mm sur bois hydrofuge. Surface mate, antireflet, offrant une excellente résistance aux chocs mécaniques.
Laboratoires de contrôle, de physique et supports d'instruments. Non recommandé pour l'usage de substances agressives.
Trespa®
Résine synthétique durcie et renforcée de 8 mm sur bois hydrofuge. Extrêmement durable et résistante aux impacts.
Utilisation générale en laboratoire (physique, contrôle, etc.). Similaire à la résine compacte, peu recommandé pour les agents chimiques agressifs.
Grès étiré
Carreaux de grès de 8 mm sur support bois hydrofuge mélaminé de 22 mm. Présente une excellente résistance chimique.
Laboratoires de chimie et milieux d'enseignement où l'exposition aux produits chimiques est élevée.
2.2.7 Conditionnement électrique
L'installation électrique d'un laboratoire doit garantir la continuité du travail et la sécurité des personnes et des équipements :
• Approvisionnement fiable et continu en énergie : réseau secteur + groupe électrogène + système d'alimentation solaire (en complément) ;
• Courant alternatif monophasé 220 V pour les équipements standards, triphasé 380 V pour les équipements à forte puissance (autoclaves, étuves à grande capacité) ;
• Dispositifs de coupure (disjoncteurs, compteurs) reconnaissables, étiquetés et facilement accessibles ;
• Suppression de toute anomalie susceptible d'affecter la sécurité de l'installation.
⚠ Sont strictement interdits :
– Conduites de fluides en hauteur traversant des installations électriques ;
– Raccordement de plusieurs blocs multiprises en série à la même fiche murale ou de paillasse ;
– Utilisation de rallonges nues branchées sur les prises de paillasse ou au sol.
2.2.8 Conditions d'ambiance
Les conditions ambiantes du laboratoire doivent permettre une exécution correcte des activités techniques. Les paramètres suivants doivent être surveillés et maîtrisés :
Tableau N°2.3 : Guide des exigences ambiantes en zone de manipulation.
Paramètre
Exigence / Recommandation
Impact si non maîtrisé
Température (T°)
Selon les exigences des équipements et méthodes analytiques (généralement 18–25°C)
Dégradation des réactifs, dérive des mesures, prolifération microbienne
Humidité relative (HR)
40–60 % pour la majorité des applications
Condensation sur les équipements, absorption des produits hygroscopiques
Éclairage
300–500 lux sur les plans de travail (norme NF EN 12464)
Erreurs de lecture, fatigue oculaire, accidents
Stérilité biologique
Maintien d'une charge microbienne aérienne conforme (classe ISO selon l'activité)
Contaminations des échantillons, faux positifs
Perturbations électromagnétiques
Blindage des équipements sensibles (spectromètres, électrophorèse)
Dérive des mesures analytiques
Bruit et vibrations
< 65 dB sur les postes de travail
Perturbation des balances analytiques, stress du personnel
-
QuizOpened: Saturday, 4 April 2026, 12:55 PMCloses: Thursday, 9 April 2026, 12:55 PM
-
République Algérienne Démocratique et Populaire
Ministère de l'Enseignement Supérieur et de la Recherche Scientifique
Centre Universitaire Nour Bachir – El-Bayadh
Département des Sciences Biologiques
Organisation & Gestion des Laboratoires
Licence 3 – Microbiologie, Biotechnologie & Biochimie | Semestre VI
PARTIE 3 — Matériel
Appareillage et consommables par type de laboratoire
Dr. NAIMI Mostefa
Maître de Conférences A – Département des Sciences Biologiques
Année universitaire 2025–2026
Partie 3 — Matériel
3.1 Appareillage par type de laboratoire
3.1.1 Laboratoire de Physicochimie
L'appareillage principal d'un laboratoire de physicochimie comprend :
• Distillateur d'eau (mono et bi-distillation) — pour la production d'eau de qualité analytique ;
• Balances analytiques (précision ±0,1 mg) et balances de précision ;
• pH-mètre avec électrode combinée et sonde de température ;
• Conductimètre pour la mesure de la conductivité électrique des solutions ;
• Polarimètre — mesure du pouvoir rotatoire des substances optiquement actives ;
• Réfractomètre — mesure de l'indice de réfraction (teneur en sucre, concentration) ;
• Spectrophotomètre UV-Visible — mesure de l'absorbance à différentes longueurs d'onde ;
• Photomètre de flamme — dosage des métaux alcalins (Na, K) par émission ;
• Four moufle — incinération des échantillons (détermination des cendres) ;
• Étuve à convection forcée — séchage, détermination de la teneur en eau ;
• Bain-marie avec agitation — réactions à température contrôlée ;
• Distillateur d'azote, soxhlet, rotavapeur — techniques de distillation et d'extraction ;
• Hotte d'aspiration chimique — protection contre les vapeurs toxiques ;
• Appareil de filtration (membrane, Büchner) — séparation par filtration.

Figure N°3.1 : Unité de distillation semi-automatique (Méthode Kjeldahl), Schéma de fonctionnement.

Figure N°3.2 : Hotte aspirante de laboratoire.
3.1.2 Laboratoire de Biochimie
En plus des équipements de physicochimie, un laboratoire de biochimie dispose de :
• Centrifugeuse réfrigérée — séparation des constituants par force centrifuge ;
• Lyophilisateur — déshydratation par sublimation (conservation des biomolécules) ;
• Concentrateur (speed-vac) — évaporation rapide sous vide ;
• Microscope optique et loupe binoculaire ;
• Appareil d'électrophorèse (SDS-PAGE, agarose) — séparation des protéines et des acides nucléiques ;
• Chromatographe : HPLC (haute performance) et CPG (phase gazeuse) ;
• Système ELISA (enzyme-linked immunosorbent assay) — dosages immunoenzymatiques ;
• Spectromètre de masse (couplé HPLC-MS/MS dans les laboratoires avancés) ;
• Automates d'analyse biochimique (Konelab, Cobas, etc.) ;
• Banque de sang (centrifugeuse de référence et réfrigérateur dédié).

Figure N°3.3 : Dispositif d'analyse par méthode ELISA (Enzyme-Linked Immunosorbent Assay).
3.1.3 Laboratoire de Microbiologie
L'appareillage spécifique d'un laboratoire de microbiologie inclut :
• Poste de Sécurité Microbiologique (PSM) de classe I, II ou III selon le niveau de confinement requis (NSB 1 à 4) ;
• Incubateur(s) à différentes températures (30°C, 35°C, 37°C, 42°C, 44°C) ;
• Étuve Pasteur (four de Pasteur = stérilisation air chaud 170°C / 1h) ;
• Autoclave (stérilisation vapeur d'eau saturée 121°C / 15 min, ou 134°C / 18 min) ;
• Bain-marie ;
• Stomacher (broyeur péristaltique pour la préparation des échantillons alimentaires) ;
• Répartiteur de milieux de culture (automatisé) ;
• Compteur de colonies (manuel avec loupe ou automatique avec analyse d'image) ;
• Ensemenceur en spirale (Archimedes spiral plater) — dénombrement de micro-organismes ;
• Thermocycleur (PCR conventionnelle, PCR en temps réel qPCR) ;
• Rampe de filtration mono ou multiposte (dénombrement sur membrane filtrante) ;
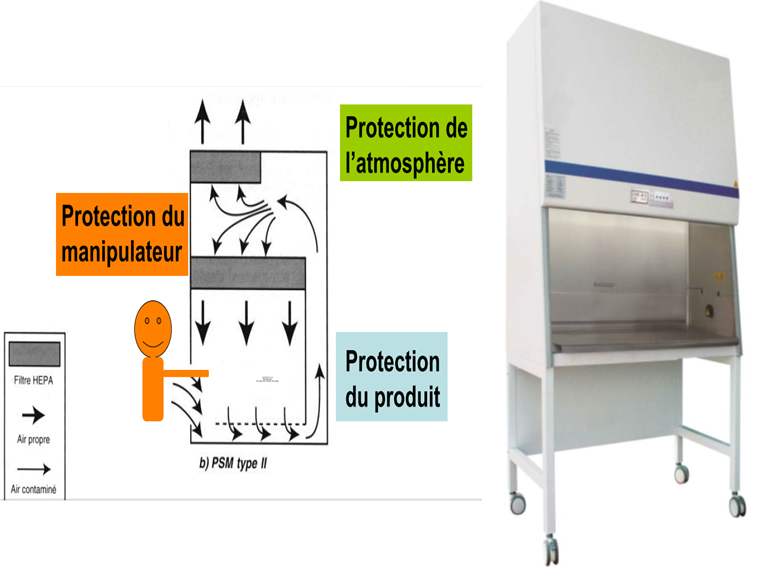
Figure N°3.4 : PSM type II : protection du manipulateur, du produit et de l'environnement, mécanisme de filtration HEPA et circulation de l'air.

Figure N°3.5 : Rampe de filtration sous vide : composants et protocoles d'utilisation.

Figure N°3.6 : Appareil de PCR : vue du bloc thermique et de l'unité de commande.
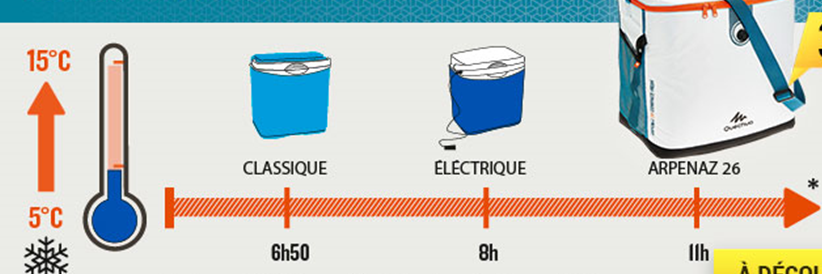
Figure N°3.7 : Comparaison entre glacières classiques, électriques et haute performance.
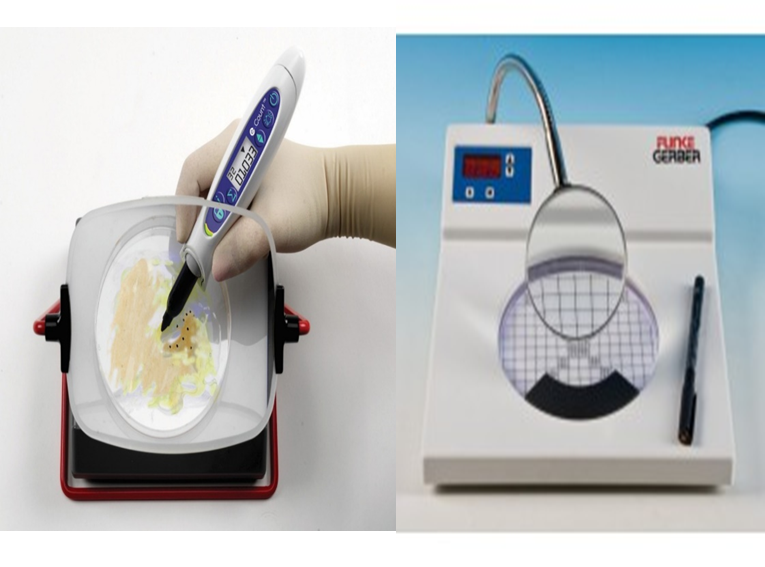
Figure N°3.8 : Compteur de colonies manuel et semi-automatique.

Figure N°3.9 : Comparaison entre l'ensemencement classique et la méthode Spiral®.
Tableau N°3.1 : Classification des Niveaux de confinement et risques biologiques (NSB1-4).
Niveaux de sécurité biologique (NSB) — Rappel
• NSB 1 : agents biologiques sans risque pour l'homme adulte sain (E. coli K12, S. cerevisiae) ;
• NSB 2 : agents pathogènes modérés (S. aureus, Salmonella, HBV) — PSM de classe II requis ;
• NSB 3 : agents à risque élevé par voie aérienne (M. tuberculosis, VIH) — PSM classe III, confinement ;
• NSB 4 : agents à risque vital sans traitement connu (Ebola) — laboratoire P4, combinaison de protection.
3.2 Consommables par type de laboratoire
3.2.1 Laboratoire de Physicochimie
La verrerie et les petits consommables comprennent :
• Verrerie volumétrique : béchers, fioles jaugées, erlens, pipettes graduées et volumétriques, micropipettes, burettes, pycnomètres, butyromètres, densimètres, alcoomètres, lactodensimètres ;
• Petits matériels : statif + noix + pinces, spatules, capsules (verre, porcelaine, platine), verres de montres, mortier et pilon ;
• EPI : pissettes (alcool, eau distillée), gants nitrile, bavette, lunettes de protection ;
• Produits chimiques : (acides et dérivés, alcools et dérivés, colorants et indicateurs).
3.2.2 Laboratoire de Biochimie
• Verrerie spécifique : cellules de numération (Mallassez, Thomas, Potain), lames et lamelles, tubes à essai à hémolyse et Eppendorf, cuves de coloration ;
• EPI : gants médicaux, bavette, coiffe, lunettes de protection ;
• Glacières avec accumulateurs de froid (transport des échantillons) ;
• Réactifs biochimiques : albumine, alpha-amylase, calcium, chlorures, cholestérol, créatinine, fer, glucose, hémoglobine, phosphatases acide et alcaline, protéines totales et urinaires, sodium, potassium, triglycérides, urée...
3.2.3 Laboratoire de Microbiologie
• Boîtes de Pétri (verre ou plastique à usage unique) ;
• Sacs stomacher pour homogénéisation des échantillons solides ;
• Filtres membrane (0,2 µm, 0,45 µm) et supports de filtration ;
• Lames et lamelles, tubes à essai, tubes Eppendorf ;
• Milieux de culture (liste non exhaustive) :
– Gélose pour dénombrement général : PCA (Plate Count Agar) ;
– Milieux sélectifs entérobactéries : VRBL (Violet Red Bile Lactose), BCP (Bromocresol Purple) ;
– Milieux Staphylocoques : Baird-Parker (BP), Chapman (MSA) ;
– Milieux Salmonelles-Shigelles : SS (Salmonella-Shigella agar), Hektoen ;
– Milieux levures et moisissures : OGA (glucosée oxytétracycline) ;
– Milieux Enterocoques : Slanetz et Bartley ;
– Milieux anaérobies : gélose viande-foie (VF), Schaedler.

Figure N°3.10 : Laveur-désinfecteur automatique pour verrerie de laboratoire.

Figure N°3.11 : Supports d'égouttage (égoutoires) pour verrerie de laboratoire.

Figure N°3.12 : Instrumentation pour le broyage et l'homogénéisation des échantillons.
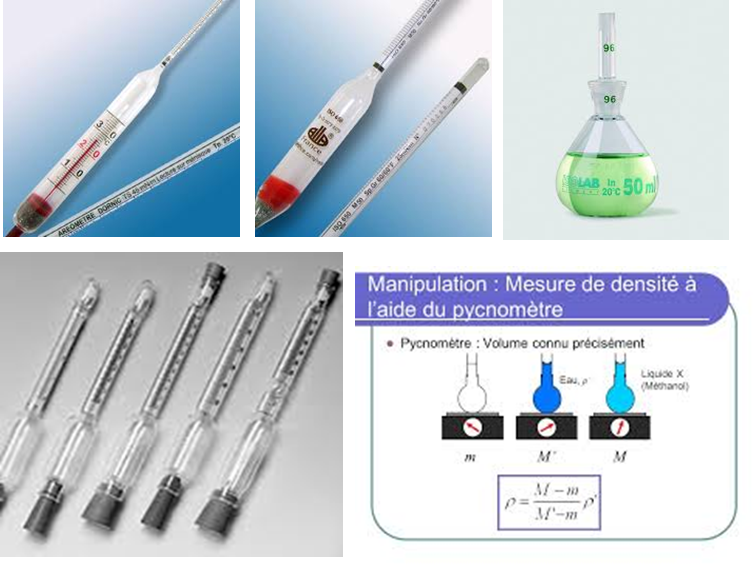
Figure N°3.13 : Instrumentation pour la mesure de la densité et de la masse volumique, aéromètres, lactodensimètres et pycnomètre.

Figure N°3.14 : Caractérisation et structure microscopique des différents types de membranes filtrantes.
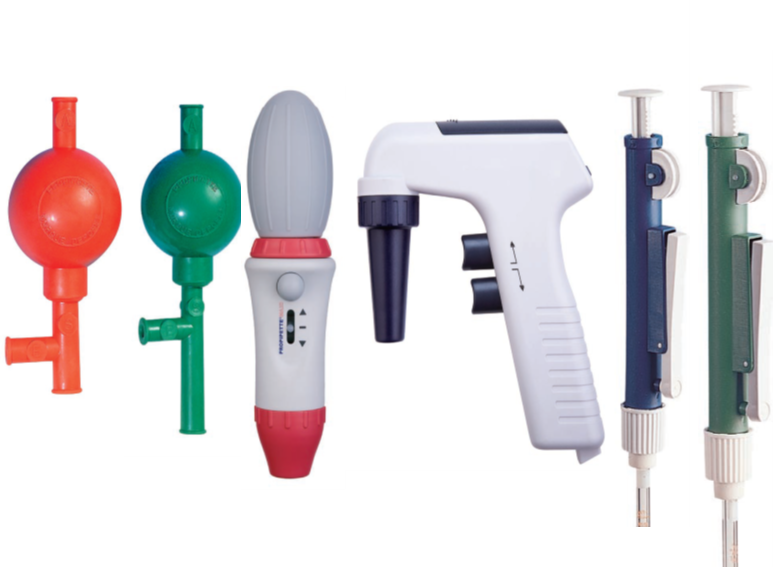
Figure N°3.15 : Dispositifs de pipetage : de la poire en caoutchouc au pipeteur électronique.

Figure N°3.16 : Organisation du tri et de la collecte des déchets de verrerie.
-
QuizOpened: Saturday, 4 April 2026, 1:12 PMCloses: Thursday, 9 April 2026, 1:12 PM
-
République Algérienne Démocratique et Populaire
Ministère de l'Enseignement Supérieur et de la Recherche Scientifique
Centre Universitaire Nour Bachir – El-Bayadh
Département des Sciences Biologiques
Organisation & Gestion des Laboratoires
Licence 3 – Microbiologie, Biotechnologie & Biochimie | Semestre VI
PARTIE 4 — Produits de laboratoire
Types, conditionnement, étiquetage, stockage sécurisé
Dr. NAIMI Mostefa
Maître de Conférences A – Département des Sciences Biologiques
Année universitaire 2025–2026
Partie 4 — Produits de laboratoire
4.1 Types de produits
4.1.1 Milieux de culture
Les milieux de culture se présentent sous trois formes commerciales :
• Milieux complets prêts à l'emploi (flacons, tubes, boîtes) à l'état liquide, solide ou semi-solide ;
• Milieux déshydratés à reconstituer au laboratoire par pesée et hydratation selon les instructions du fabricant ;
• Ingrédients déshydratés à mélanger au laboratoire selon des formules définies (milieux maison).
4.1.2 Produits chimiques
Les produits chimiques se présentent sous diverses formes physiques (liquide, solide) et concentrations :
• Acides (chlorhydrique, sulfurique, nitrique, acétique, trichloroacétique, etc.) ;
• Bases (soude, potasse, ammoniaque, etc.) ;
• Alcools (éthanol, méthanol, isopropanol, etc.) ;
• Sels, tampons, solvants organiques.
4.1.3 Réactifs
Les réactifs comprennent :
• Anticorps (polyclonaux et monoclonaux) pour les techniques d'immunoanalyse ;
• Antigènes pour les tests sérologiques ;
• Sondes nucléiques pour les techniques de biologie moléculaire (PCR, hybridation) ;
• Colorants et indicateurs de couleur (érythrosine, violet de gentiane, éosine, safranine...) ;
• Étalons certifiés et solutions tampons pH calibrés ;
• Substrats enzymatiques pour les dosages enzymatiques.
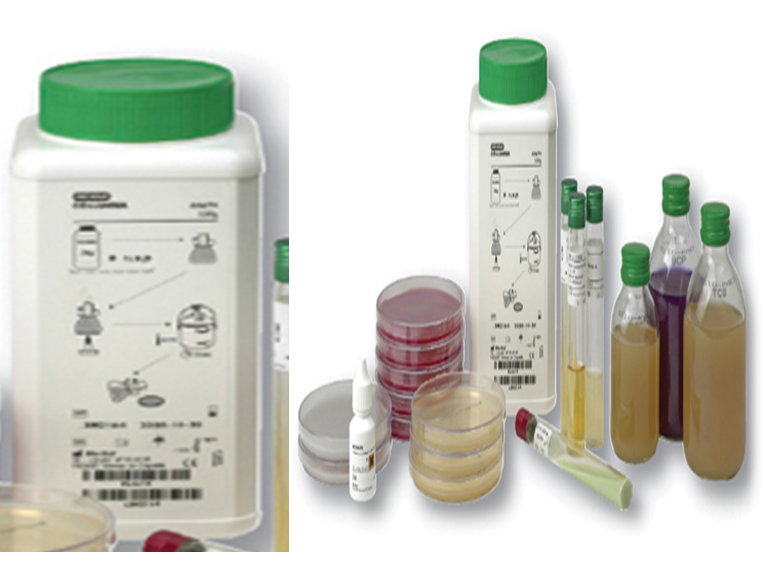
Figure N°4.1 : Produits de laboratoire, milieux de culture.

Figure N°4.2 : Produits de laboratoire, produits chimiques.
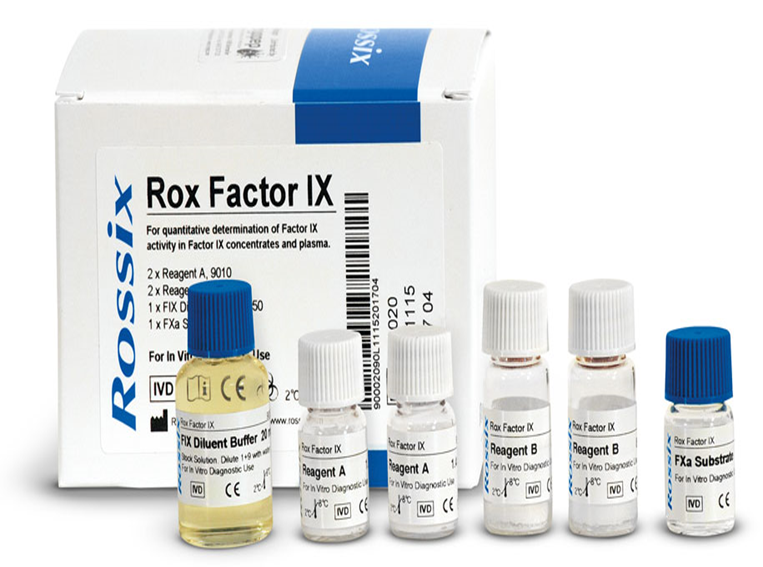
Figure N°4.3 : Produits de laboratoire, réactives.
4.2 Conditionnement
Le conditionnement doit protéger le produit de toute altération et être adapté à sa nature :
Tableau N°4.1 : Type de conditionnement, avantages et applications typiques.
Type de conditionnement
Avantages
Applications typiques
Flacons en verre ambré
Opaque → protection des produits photosensibles
Réactifs peroxydables, colorants, solutions instables à la lumière
Flacons en verre transparent
Contrôle visuel du contenu et de la couleur
Acides, bases concentrées, solvants stables
Flacons en plastique (PE, PP, HDPE)
Légers, résistants aux chocs, moins coûteux
Solutions aqueuses, milieux de culture, tampons
Flacons en aluminium
Protection maximale contre la lumière et l'humidité
Produits très sensibles, poudres hygroscopiques

Figure N°4.4 : Type de conditionnement, Polymère en plastique, Aluminium, verre transparent translucide et ambré.
4.3 Étiquetage
L'étiquette est une source primordiale d'informations. Elle est obligatoire sur tout flacon ou contenant et doit mentionner :
• Nom et coordonnées du fabricant ou fournisseur ;
• Dénomination commerciale du produit, formule chimique (pour les produits chimiques) et titre/concentration ;
• Dates : de réception au laboratoire, de première utilisation, de préparation ou reconstitution, de fabrication et de péremption ;
• Contenance (pour les liquides) ou masse (pour les solides) ;
• Mode d'utilisation et/ou de préparation ;
• Composition (ingrédients) et degré de pureté (pour les produits chimiques) ;
• Certificats de conformité et de contrôle qualité ;
• Fiche de données de sécurité (FDS/SDS) — référence ou accès ;
• Pictogrammes de danger selon le Système Général Harmonisé (SGH/GHS) :

Figure N°4.5 : Etiquetage, une importante d'informations.
Tableau N°3.1 : Pictogramme de risque et signification.
Pictogramme
Signification
Pictogramme
Signification
🔥
Inflammable
☠
Toxique (aigu)
⚠
Nocif / Irritant
⊛
Oxydant / Comburant
🧪
Corrosif
♻
Dangereux pour l'environnement
4.4 Stockage des produits de laboratoire
4.4.1 Localisation du stockage
Le stockage des produits de laboratoire s'organise en deux niveaux complémentaires :
• Local de stockage extérieur (central) : isolé du reste du bâtiment, à porte anti-feu, destiné au stockage de grande capacité à moyen ou long terme. Il doit être bien ventilé, bien éclairé et à accès contrôlé ;
• Local de stockage intérieur (tampon) : situé dans le laboratoire, réservé aux besoins à court terme et aux produits en cours d'utilisation.

Figure N°4.6 : Endroit de stockage : stockage intérieur et de stockage extérieur.
4.4.2 Conditions de conservation
Les conditions de conservation doivent être respectées en fonction des caractéristiques physicochimiques des produits :
Tableau N°3.1 : Conditions de conservation, facteurs, produits concerné et mesure de protection.
Facteur d'altération
Produits concernés
Mesure de protection
Humidité
Produits hygroscopiques, hydrolysables, métaux alcalins
Conservation en flacon hermétique, dessiccateur, armoire climatisée
Chaleur
Produits sublimables, peroxydables, polymérisables
Réfrigération (2–8°C) ou congélation (–20°C ou –80°C)
Froid
Produits cristallisables, gélifiables, émulsions
Conserver à température ambiante contrôlée (15–25°C)
Lumière (UV)
Produits photosensibles, peroxydables, polymérisables
Flacons ambrés, armoires opaques, obscurité
Oxygène de l'air
Produits oxydables, poudres métalliques
Conditionnement sous atmosphère inerte (azote, argon)

Figure N°4.7 : Endroit de stockage, armoires ventilé, rayonnage, caissons
4.4.3 Règles de stockage
Les règles fondamentales de stockage des produits de laboratoire sont :
• Ne jamais mélanger le stockage du matériel et celui des produits chimiques ;
• Ne jamais stocker ensemble des produits chimiques incompatibles (risque de réactions violentes en cas de fuite ou d'évaporation) ;
• Stocker une quantité minimale de produits, proportionnelle à l'activité du laboratoire ;
• Appliquer la règle PEPS (Premier Entré, Premier Sorti = FIFO) ;
• Tenir à jour une liste des produits toxiques (quantité et localisation) ;
• Proscrire le stockage à proximité des extincteurs, des douchettes de sécurité et des sorties de secours ;
• Accès contrôlé aux personnes spécialement formées et désignées (ingénieur de laboratoire, responsable qualité) ;
• Gestion informatisée s'inspirant des procédures d'assurance qualité.
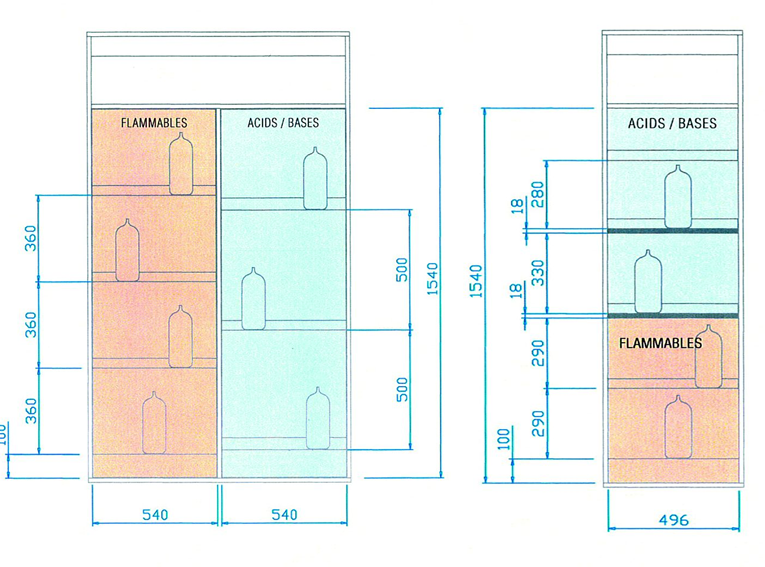
Figure N°4.9 : Schémas de stockage pour produits, acides/Bases et inflammables.


Figure N°4.9 : Extincteurs et douchettes de sécurité.
-
QuizOpened: Saturday, 4 April 2026, 1:18 PMCloses: Thursday, 9 April 2026, 1:18 PM
-
République Algérienne Démocratique et Populaire
Ministère de l'Enseignement Supérieur et de la Recherche Scientifique
Centre Universitaire Nour Bachir – El-Bayadh
Département des Sciences Biologiques
Organisation & Gestion des Laboratoires
Licence 3 – Microbiologie, Biotechnologie & Biochimie | Semestre VI
PARTIE 5 — Personnel
Qualifications, fonctions, formation continue, hygiène
Dr. NAIMI Mostefa
Maître de Conférences A – Département des Sciences Biologiques
Année universitaire 2025–2026
Partie 5 — Personnel
Le personnel est l'élément le plus important de l'organisation d'un laboratoire. Un laboratoire ne peut fonctionner sans un personnel adéquatement formé et, pour certains essais, possédant une qualification professionnelle reconnue.
5.1 Qualifications du personnel
La qualification du personnel associe deux composantes complémentaires :
Tableau N°5.1 : Qualifications du personnel, aptitudes de base et des compétences.
Aptitudes (composante 1)
Les aptitudes sont établies sur la base d'un ou plusieurs des éléments suivants :
– Un diplôme, savoir, professionnel ou académique reconnu (technicien, ingénieur, biologiste médical, pharmacien...) ;
– Une expérience professionnelle prouvée (ancienneté dans la fonction, portfolio de compétences) ;
– Une formation spécifique externe (organisme de formation accrédité) ou interne (compagnonnage, tutorat).
Compétences (composante 2)
Les compétences correspondent au savoir-faire et savoir-être opérationnel, évalué selon trois niveaux :
– Niveau utilisateur : exécution des tâches courantes sous supervision ;
– Niveau maîtrise : exécution autonome et formation des utilisateurs ;
– Niveau expert : conception, validation de méthodes, audit interne.
Exemples de compétences évaluables : réalisation d'examens sur équipement donné, prélèvements particuliers, maintenance sur équipement donné, validation de comptes rendus avec interprétation, élaboration et validation de méthodes, encadrement, etc.
 Figure N°5.1 :
Figure N°5.1 : Diagramme circulaire de trois piliers fondamentaux de la qualification professionnelle, (1) formation, (2) expérience et (3) compétences démontrées.
5.2 Définitions de fonctions
Chaque fonction dans le laboratoire doit être formellement définie dans un document intitulé « fiche de poste » ou « description de fonction ». Ce document précise :
• L'intitulé de la fonction (ingénieur de laboratoire, technicien supérieur, biologiste médical, responsable qualité, secrétaire, aide de laboratoire, personnel d'entretien, etc.) ;
• Les activités, missions et tâches spécifiques associées ;
• Les responsabilités et autorités (décision, signature, validation) ;
• Les relations hiérarchiques et fonctionnelles (organigramme) ;
• Le règlement interne et le statut particulier applicable.
5.3 Formation continue et développement professionnel
Le laboratoire doit assurer à l'ensemble de son personnel une formation continue en quantité et qualité suffisantes. Les preuves de cette formation doivent être documentées et incluent :
• Lecture de références bibliographiques (revues scientifiques, normes, guides techniques) ;
• Formation individuelle présentielle ou à distance (e-learning, MOOC) ;
• Participation à des manifestations scientifiques (congrès, séminaires, journées techniques) ;
• Réunions de staff et réunions de service (partage d'expériences, retour sur incidents) ;
• Contrôles de qualité internes et participation aux essais inter-laboratoires (EIL) ;
• Habilitations spécifiques renouvelables (manipulation de produits dangereux, techniques spécialisées).
5.4 Hygiène du personnel
Dans le domaine de l'hygiène du personnel, les précautions suivantes sont obligatoires pour éviter la contamination des échantillons et les risques d'infection du personnel :
• Porter des vêtements de laboratoire correctement fermés, propres et en bon état, dans un tissu limitant les risques d'inflammabilité (blouse en coton ou mélange ignifugé) ;
• Porter les équipements de protection individuelle (EPI) : gants adaptés au risque, coiffe pour les cheveux ;
• Garder des ongles propres, de préférence courts et sans vernis (risque de perforation des gants) ;
• Se laver soigneusement les mains à l'eau tiède avant et après les examens microbiologiques, et immédiatement après chaque passage aux toilettes, distribuée de préférence par un robinet à commande non manuelle ;
• Utiliser un savon liquide ou désinfectant ; se sécher avec des serviettes en papier à usage unique ;
• Pendant le travail avec des échantillons ou des cultures contaminés : éviter de parler, de tousser et d'éternuer en direction du poste de travail ;
• Ne pas fumer, manger ni boire dans le laboratoire ; ne pas placer d'aliments dans les réfrigérateurs du laboratoire ;
• Le pipetage à la bouche est formellement et définitivement proscrit.
-
QuizOpened: Saturday, 4 April 2026, 1:25 PMCloses: Thursday, 9 April 2026, 1:25 PM
-
Partie 6— Dangers et risques : Types de risques (physiques, biologiques, chimiques), moyens de lutte.
République Algérienne Démocratique et Populaire
Ministère de l'Enseignement Supérieur et de la Recherche Scientifique
Centre Universitaire Nour Bachir – El-Bayadh
Département des Sciences Biologiques
Organisation & Gestion des Laboratoires
Licence 3 – Microbiologie, Biotechnologie & Biochimie | Semestre VI
PARTIE 1 — Dangers et Risques dans les Laboratoires
Types de risques (physiques, biologiques, chimiques), moyens de lutte
Dr. NAIMI Mostefa
Maître de Conférences A – Département des Sciences Biologiques
Année universitaire 2025–2026
Partie 6 — Dangers et risques dans les laboratoires
6.1 Types de risques
Les risques existant dans les laboratoires des sciences de la nature et de la vie (microbiologie, biochimie, chimie...) sont de trois natures : physiques, biologiques et chimiques.
6.1.1 Risques physiques
Les risques physiques proviennent essentiellement du non-respect des normes de construction et d'installation :
• Inondation : rupture de canalisations d'eau, dégâts des eaux en cas de défaillance du réseau hydraulique ;
• Électrocution et électrisation : câbles dénudés, prises défectueuses, utilisation non conforme des appareils électriques ;
• Introduction de germes extérieurs, de poussières et de nuisibles (rongeurs, insectes) en cas de non-étanchéité ou de fissures dans la structure bâtie ;
• Accidents liés à l'utilisation incorrecte des équipements par méconnaissance du principe de fonctionnement ;
• Risques incendie et explosion liée à la présence de produits inflammables ou d'équipements sous pression.
6.1.2 Risques biologiques
Dans un laboratoire de sciences de la nature et de la vie, les manipulations de base impliquent le transfert d'échantillons biologiques soupçonnés d'altération ou de contamination. Ces manipulations doivent prévenir trois types de contaminations :
Tableau N°6.1 : Type de contamination et conséquence.
Type de contamination
Direction du transfert
Conséquence
Du produit vers le manipulateur
Produit → Personnel
Infection professionnelle, maladie occupationnelle
Du manipulateur vers le produit
Personnel → Produit
Faux positifs, résultats non fiables, invalidation de l'analyse
Du produit vers l'environnement
Produit → Environnement
Contamination de l'espace de travail, risque pour les tiers
6.1.3 Risques chimiques
Les risques chimiques dans les laboratoires de sciences de la nature et de la vie sont liés aux produits chimiques et aux réactifs connexes utilisés pour les analyses physicochimiques et biochimiques. Le personnel peut être exposé aux risques suivants :
• Cancers : exposition à des substances cancérigènes, mutagènes et reprotoxiques (CMR) (benzène, formaldéhyde, bromure d'éthidium, aflatoxines...) ;
• Destruction brutale des tissus : substances corrosives (acides concentrés, bases fortes, oxydants puissants) ;
• Irritation des voies respiratoires, oculaires et cutanées : substances irritantes (acide acétique, ammoniaque, chlore...) ;
• Incendie et explosion : substances inflammables (alcools, solvants organiques, gaz comprimés).
6.2 Moyens de lutte et prévention
La prévention des risques en laboratoire repose sur une approche hiérarchique (supprimer > réduire > protéger) et sur l'application rigoureuse des règles suivantes :
• Personnel qualifié, sensibilisé aux risques et donnant l'exemple de la bonne pratique ;
• Application stricte des règles de bonnes pratiques de laboratoire (BPL) et d'hygiène du personnel ;
• Fermeture hermétique des portes et fenêtres pour éviter l'introduction de germes extérieurs, poussières et nuisibles ;
• Nettoyage et désinfection systématiques de tous les outils et surfaces après manipulation ;
• Assurance du bon fonctionnement des appareils par maintenance préventive régulière ;
• Affichage visible des fiches signalétiques à l'entrée du laboratoire et à proximité des produits dangereux ;
• Respect scrupuleux des conseils d'utilisation des produits chimiques et des pictogrammes réglementaires ;
• Vaccination du personnel exposé aux agents biologiques (hépatite B, tétanos, grippe...) ;
• Présence et entretien des matériels de secours : extincteurs adaptés, douche de sécurité, lave-œil, pharmacie de premier secours ;
• Organisation de visites médicales systématiques et périodiques du personnel ;
• Formation régulière aux risques et organisation de tables rondes de retour d'expérience.
Tableau N°6.1 : Gestion des déchets : Conformité au décret exécutif n° 03-478.
⚠ Gestion des déchets de laboratoire
Les déchets de laboratoire doivent être gérés selon la réglementation nationale (décret exécutif n° 03-478 sur les DASRI en Algérie) :
• DASRI (Déchets d'Activités de Soins à Risques Infectieux) : traitement par autoclavage puis filière d'élimination agréée ;
• Déchets chimiques : filière agréée selon la nature (oxydants, inflammables, CMR) — ne jamais rejeter à l'évier ;
• Déchets piquants-coupants : conteneurs rigides à usage unique (sharps containers) ;
• Déchets radioactifs (si activité concernée) : déclaration obligatoire, filière spécialisée.
-
QuizOpened: Saturday, 4 April 2026, 1:33 PMCloses: Thursday, 9 April 2026, 1:33 PM
-
République Algérienne Démocratique et Populaire
Ministère de l'Enseignement Supérieur et de la Recherche Scientifique
Centre Universitaire Nour Bachir – El-Bayadh
Département des Sciences Biologiques
Organisation & Gestion des Laboratoires
Licence 3 – Microbiologie, Biotechnologie & Biochimie | Semestre VI
PARTIE 1 — Conformité aux Normes Algériennes et Internationales
Normes algériennes et internationales applicables
Dr. NAIMI Mostefa
Maître de Conférences A – Département des Sciences Biologiques
Année universitaire 2025–2026
Partie 7 — Conformité aux normes algériennes et internationales
7.1 Le système algérien de normalisation et d'accréditation
7.1.1 L'IANOR — Institut Algérien de Normalisation
L'IANOR (Institut Algérien de Normalisation) est l'organisme national de normalisation en Algérie. Créé par le décret exécutif n° 98-69 du 21 février 1998, il est chargé de :
• Élaborer, approuver et diffuser les normes algériennes (NA) ;
• Représenter l'Algérie auprès des organismes internationaux de normalisation (ISO, CEN, CODEX ALIMENTARIUS) ;
• Assurer la transposition des normes internationales en normes algériennes.
7.1.2 ALGERAC — Organisme Algérien d'Accréditation
L’ALGERAC (Organisme Algérien d'Accréditation) est l'organisme national d'accréditation en Algérie, créé par le décret exécutif n° 05-466. Il délivre les accréditations aux :
• Laboratoires d'essais et d'étalonnage (selon ISO/CEI 17025) ;
• Laboratoires médicaux (selon ISO 15189) ;
• Organismes d'inspection et de certification.
L'accréditation ALGERAC constitue la reconnaissance officielle de la compétence technique d'un laboratoire en Algérie.
7.1.3 Le Journal Officiel de la République Algérienne (JORA)
Les textes réglementaires algériens encadrant les laboratoires incluent notamment :
• Décret exécutif n° 03-478 du 9 décembre 2003 relatif aux déchets d'activités de soins à risques infectieux et assimilés (DASRI) ;
• Arrêté interministériel relatif aux bonnes pratiques de laboratoire (BPL) ;
• Loi n° 18-11 du 2 juillet 2018 relative à la santé (dispositions sur les laboratoires d'analyses médicales).
7.2 Normes applicables aux analyses
7.2.1 Analyses microbiologiques
Les analyses microbiologiques dans les laboratoires algériens doivent être conformes aux normes suivantes :
Norme
Objet
Application
ISO 4833
Dénombrement des microorganismes — Technique par comptage de colonies
Contrôle microbiologique des aliments et de l'eau
ISO 21528
Recherche et dénombrement des Enterobacteriaceae
Contrôle hygiénique des aliments transformés
ISO 6888
Dénombrement des Staphylocoques à coagulase positive
Détection de contamination d'origine humaine
ISO 6579
Recherche des Salmonella
Contrôle des aliments et des environnements de production
ISO 11290
Recherche et dénombrement de Listeria monocytogenes
Contrôle des aliments réfrigérés, charcuteries
ISO 16649
Dénombrement d'E. coli β-glucuronidase positive
Indicateur de contamination fécale
NA 1200 (JORA)
Normes algériennes microbiologiques des aliments
Critères légaux en vigueur en Algérie
7.2.2 Analyses physicochimiques
Les méthodes de référence pour les analyses physicochimiques sont définies par :
• Les normes ISO et EN transposées en normes algériennes NA par l'IANOR ;
• Les méthodes officielles du JORA (pour les analyses légales) ;
• Les méthodes AOAC (Association of Official Analytical Chemists) pour les analyses agroalimentaires ;
• Les méthodes de la Pharmacopée Européenne pour les analyses pharmaceutiques.





-
République Algérienne Démocratique et Populaire
Ministère de l'Enseignement Supérieur et de la Recherche Scientifique
Centre Universitaire Nour Bachir – El-Bayadh
Département des Sciences Biologiques
Organisation & Gestion des Laboratoires
Licence 3 – Microbiologie, Biotechnologie & Biochimie | Semestre VI
PARTIE 1 — Normes Internationales en Vigueur
ISO 15189, ISO 17025, OMS, ALGERAC, accréditation
Dr. NAIMI Mostefa
Maître de Conférences A – Département des Sciences Biologiques
Année universitaire 2025–2026
Partie 8 — Normes internationales en vigueur
8.1 ISO/CEI 17025 — Laboratoires d'essais et d'étalonnage
Présentation de la norme ISO/CEI 17025 :2017
La norme ISO/CEI 17025 spécifie les exigences générales de compétence pour réaliser des essais et des étalonnages, y compris l'échantillonnage. Elle s'applique à tous les laboratoires, quelle que soit leur taille et leur domaine d'activité.
La norme ISO/CEI 17025 :2017 est organisée en deux blocs d'exigences :
8.1.1 Exigences relatives au management
• Organisation et management du système de management (direction, politique qualité, objectifs) ;
• Maîtrise de la documentation (procédures, modes opératoires, enregistrements) ;
• Maîtrise des enregistrements ;
• Actions correctives et préventives ;
• Audit interne et revue de direction ;
• Gestion des réclamations et des non-conformités.
8.1.2 Exigences techniques
• Personnel : compétence, qualification, habilitation, formation continue ;
• Locaux et conditions ambiantes : conformité aux exigences de la méthode ;
• Méthodes d'essai et d'étalonnage : validation, vérification, estimation de l'incertitude ;
• Équipements : étalonnage, vérification, maintenance, traçabilité métrologique ;
• Traçabilité des mesures aux étalons nationaux/internationaux ;
• Echantillonnage et manutention des objets d'essai et d'étalonnage ;
• Assurance qualité des résultats d'essai et d'étalonnage ;
• Rapport sur les résultats.
8.2 ISO 15189 — Laboratoires de biologie médicale
Présentation de la norme ISO 15189 :2022
La norme ISO 15189 spécifie les exigences de qualité et de compétence des laboratoires médicaux. Elle intègre des exigences spécifiques aux examens de biologie médicale (pré-analytique, analytique, post-analytique) ainsi que des exigences relatives à la sécurité des patients.
L'ISO 15189 :2022 est structurée selon le cycle PDCA (Plan-Do-Check-Act) et couvre :
• Phase pré-analytique : prescription, identification et prélèvement du patient, transport et réception des échantillons, préparation des échantillons ;
• Phase analytique : validation des méthodes analytiques, contrôles de qualité internes (CQI), participation aux contrôles qualité externes (EEQ) ;
• Phase post-analytique : validation et interprétation des résultats, transmission des résultats, gestion des urgences.
8.3 Manuel de management de la qualité de l'OMS
L'OMS (Organisation Mondiale de la Santé) a publié le « Système de gestion de la qualité au laboratoire — Manuel » (OMS, Genève, 2013), qui constitue le cadre de référence pour les laboratoires de santé dans les pays en développement. Il est organisé autour de 12 éléments de qualité :
N°
Élément de qualité
Contenu principal
1
Organisation
Structure organisationnelle, responsabilités, organigramme
2
Personnel
Recrutement, qualification, formation, évaluation
3
Équipement
Sélection, installation, qualification, maintenance, étalonnage
4
Processus de travail
SOP (procédures opératoires standard), validation des méthodes
5
Documents et enregistrements
Maîtrise documentaire, traçabilité des résultats
6
Gestion de l'information
Système d'information de laboratoire (LIS), confidentialité
7
Gestion des incidents
Signalement, analyse des causes, actions correctives
8
Gestion de l'approvisionnement
Sélection des fournisseurs, réception, qualification
9
Contrôle de qualité des processus
CQI, EEQ, gestion des résultats aberrants
10
Évaluation et audit
Audit interne, revue de direction, certification
11
Amélioration continue
Actions correctives et préventives, indicateurs qualité
12
Sécurité au laboratoire
NSB, EPI, gestion des déchets, plan d'urgence
8.4 ISO 9001 :2015 — Systèmes de management de la qualité
La norme ISO 9001 :2015 est une norme généraliste applicable à tout type d'organisation, dont les laboratoires. Elle repose sur 7 principes du management de la qualité :
1. Orientation client.
2. Leadership.
3. Implication du personnel.
4. Approche processus.
5. Amélioration.
6. Prise de décision fondée sur des preuves.
7. Management des relations avec les parties intéressées.
8.5 Bonne Pratiques de Laboratoire (BPL)
Les Bonnes Pratiques de Laboratoire (BPL) constituent un ensemble de principes relatifs au processus organisationnel et aux conditions dans lesquelles les études non cliniques de sécurité sont planifiées, réalisées, contrôlées, enregistrées, archivées et rapportées. Les principes BPL couvrent :
• Organisation et personnel des installations d'essais.
• Programme d'assurance qualité.
• Locaux, appareils, matériels, réactifs.
• Systèmes d'essais.
• Substances à l'essai et substances de référence.
• Protocoles d'étude et conduite des études.
• Rapports des résultats des études.
• Archivage et conservation.





-
-
AOAC. (2023). Official methods of analysis of AOAC International (G. W. Latimer, Jr., Éd.; 22ᵉ éd.). AOAC International.
Catalogues BioLabo. https://www.biolabo.fr/
Catalogues BioMaghreb. https://www.biolabo.fr/
Catalogues LaboModerne. (2026). https://www.labomoderne.com/nos-catalogues
CLSI. (2019). Quality management system : A model for laboratory services ; Approved guideline. CLSI, 5ᵉ Édition.
Codex Alimentarius. (2023). Principes généraux d'hygiène alimentaire (CXC 1-1969). Organisation des Nations Unies pour l'alimentation et l'agriculture ; Organisation mondiale de la Santé.
COFRAC. (2021). Guide technique d'accréditation en biologie.
République algérienne démocratique et populaire. (2003). Décret exécutif nᵒ 03-478 du 15 chaoual 1424 correspondant au 9 décembre 2003 relatif aux déchets d'activités de soins à risques infectieux et assimilés. Journal officiel nᵒ 78.
République algérienne démocratique et populaire. (2018). Loi nᵒ 18-11 du 18 Chaoual 1439 correspondant au 2 juillet 2018 relative à la santé. Journal officiel nᵒ 46.
ISO 17025:2018. (2005). Exigences générales concernant la compétence des laboratoires d'étalonnage et d'essai. Organisation internationale de normalisation (ISO), Genève.
ISO 9000 :2015. Systèmes de management de la qualité – Principes essentiels et vocabulaire. ISO, Genève.
ISO 9001 : 2015. Systèmes de management de la qualité – Exigences. Organisation internationale de normalisation (ISO), Genève.
ISO 15189 : 2022. Laboratoires de biologie médicale – Exigences concernant la qualité et la compétence. Organisation internationale de normalisation (ISO), Genève.
ISO 4833. Microbiologie de la chaîne alimentaire – Méthode horizontale pour le dénombrement des microorganismes – Technique par comptage de colonies.
ISO 21528. Microbiologie de la chaîne alimentaire — Méthode horizontale pour la recherche et le dénombrement des Enterobacteriaceae.
ISO 6888. Microbiologie des aliments — Méthode horizontale pour le dénombrement des staphylocoques à coagulase positive.
ISO 6579. Microbiologie de la chaîne alimentaire — Méthode horizontale pour la recherche des Salmonella spp.
ISO 11290. Microbiologie de la chaîne alimentaire — Méthode horizontale pour la recherche et le dénombrement de Listeria monocytogenes.
ISO 16649. Microbiologie de la chaîne alimentaire – Méthode horizontale pour le dénombrement des Escherichia coli bêta-glucuronidase positive.
NA ISO 7218 : Institut algérien de normalisation (2008). Microbiologie des aliments — Exigences générales et recommandations pour les examens microbiologiques. Organisation internationale de normalisation (ISO), Genève.
Naimi, M. (2016). Cahier technique 1 : Technologie et maintenance des équipements de laboratoires des Sciences de la nature et de la vie Centre universitaire Nour Bachir El-Bayadh.
Naimi, M. (2018) Cahier technique-2 : Techniques de contrôle microbiologiques. Centre universitaire Nour Bachir El-Bayadh.
OMS. (2008). Manuel d'entretien et de maintenance des appareils de laboratoire.
OMS. (2013). Système de gestion de la qualité au laboratoire : Manuel. Genève.
