Microorganismes thérapeutiques
Topic outline
-
-
Forum
-
Forum
-
-
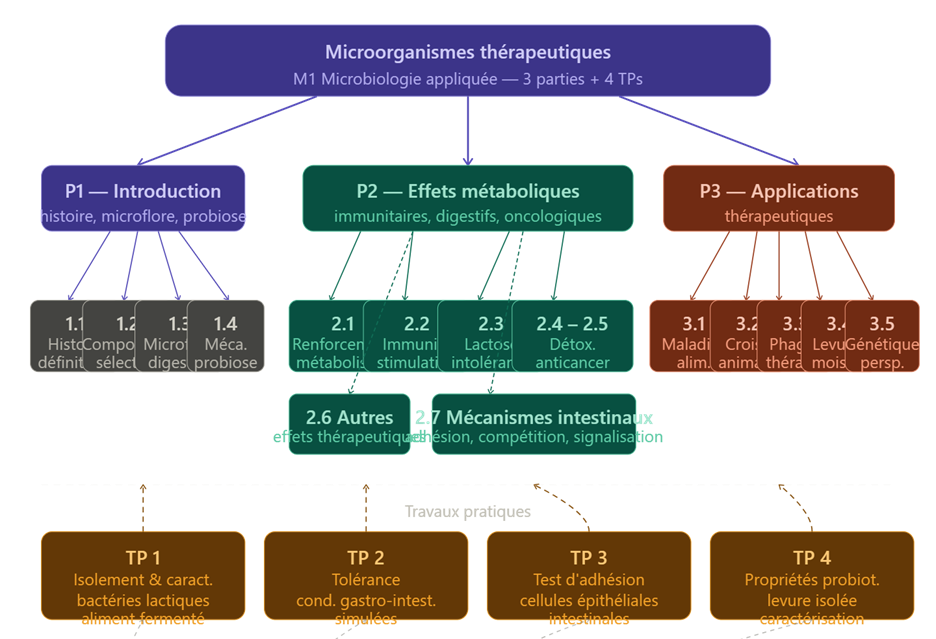
Le cours « Microorganismes thérapeutiques, M1 Microbiologie appliquée » est divisé en 3 parties :
Partie 1 : Introduction
1.1 Histoire, concepts et définitions.
1.2 Composition des probiotiques et critères de sélection.
1.3 Microflore du système digestif.
1.4 Mécanismes de probiose.
Partie 2 : Effets sur le métabolisme de l’hôte
2.1 Renforcement du métabolisme
2.2 Stimulation du système immunitaire
2.3 Probiotiques et intolérance au lactose
2.4 Détoxification
2.5 Activité anticarcinogénique
2.6 Autres effets thérapeutiques documentés
2.7 Mécanismes d'action des probiotiques dans l'intestin
Partie 3 : Applications thérapeutiques.
3.1 Prévention des maladies d'origine alimentaire.
3.2 Stimulation de la croissance des animaux.
3.3 Phagothérapie — Principes fondamentaux et applications cliniques.
3.4 Levures et moisissures à usage thérapeutique.
3.5 Amélioration génétique des souches probiotiques et perspectives.
Travaux pratiques :
TP 1 — Isolement et caractérisation des bactéries lactiques d'un aliment fermenté.
TP 2 — Évaluation de la tolérance aux conditions gastro-intestinales simulées.
TP 3 — Test d'adhésion sur cellules épithéliales intestinales.
TP 4 — Évaluation des propriétés probiotiques d'une levure isolée.
-
Dr. NAIMI Mostefa
Maître de conférences A
Département des Sciences Biologiques, bureau N°1
 m.naimi@cu-elbayadh.dz
mostecoc@yahoo.fr mosttus@yahoo.fr
m.naimi@cu-elbayadh.dz
mostecoc@yahoo.fr mosttus@yahoo.fr  https://www.researchgate.net/profile/Naimi_Mostefa
https://www.researchgate.net/profile/Naimi_Mostefa
 https://scholar.google.com/citations?hl=en&user=YG58ihMAAAAJ
https://scholar.google.com/citations?hl=en&user=YG58ihMAAAAJ https://www.facebook.com/mostecoc
https://www.facebook.com/mostecoc
-
– Chargé du cours & TP : Dr. NAIMI Mostefa.
– Intitulé de l’UE : Microorganismes thérapeutiques.
– Intitulé de la matière : Microorganismes thérapeutiques.
– Master Microbiologie appliquée.
– UE : Découverte.
– Coefficient : 2.
– Crédits : 2.
Volume horaire :
– Séance du cours (1 h 30).
– Séance TP (1 h 30).
Modalité d'évaluation :
– Examen écrit : 60 %.
– Évaluation continue : 40 % (note TD : 20 %, note TP : 20 %).
-
L’objectif de cette matière est de permettre à l’étudiant, à la fin du semestre, d’avoir des compétences sur les bienfaits des microorganismes bénéfiques pour la santé humaine et animale aussi bien que sur les mécanismes qui y sont impliqués.
– Les probiotiques, prébiotiques, postbiotiques et synbiotiques selon les définitions consensuelles actuelles (ISAPP 2021), et identifier les principaux microorganismes.
– La composition et la dynamique du microbiote intestinal humain, et les mécanismes de probiose et d'action des probiotiques sur l'hôte.
– Les effets des probiotiques sur le métabolisme de l'hôte, mécanismes et rôles.
– Les nouvelles applications thérapeutiques documentées post-2020, stratégies d'amélioration, perspectives et enjeux réglementaires et éthiques.
-
Méthodes d'enseignement
En ligne/hybride
Centré sur le travail personnel (questions, participation et prise de parole; exposés),
Afin de mieux se préparer à l'interrogation de TP et à l’examen.
Contrôle continu et examen.
Support de cours & Modalités d'évaluation
Support de cours
Fiche de consignes de rédaction de l’exposé
Lignes de conduite
Horaire et lieu (cours).
Respect.
Présence obligatoire.
Lectures complémentaires
Les ressources en ligne sont extrêmement nombreuses (sur Google par exemple, tapez « mot clé » et sélectionnez les sites les plus rigoureux).
Charalampopoulos, D., & Rastall, R. A. (Éds.). (2009). Prebiotics and probiotics science and technology. Springer.
Mojgani, N., & Dadar, M. (Éds.). (2021). Probiotic bacteria and postbiotic metabolites: Role in animal and human health. Springer.

-
La maîtrise des fondamentaux en microbiologie générale (L2) et en microbiologie industrielle (utilisation des Mos en position technologique) L3, ainsi qu'en mycologie, virologie, parasitologie, systématique (L3) et immunologie L2 est requise. Ce socle disciplinaire, correspondant aux acquis de la licence 3 et du master 1 en microbiologie, constitue un prérequis indispensable pour suivre cet enseignement.
Matière source
Connaissances requises
Niveau de maîtrise attendu
Microbiologie générale (L2)
Structure cellule procaryote/eucaryote
Classification microbienne (Gram, sporulation).
Fermentation lactique et agents impliqués.
Savoir nommer et différencier les principaux groupes : Firmicutes, Bacteroidota, Actinobacteria, Proteobacteria.
Microbiologie industrielle (L3, M1)
Fermentation industrielle et bioréacteurs
Sélection de souches d'intérêt industriel
Notion de métabolites primaires et secondaires.
Comprendre les critères de sélection d'une souche en vue d'une application industrielle ou thérapeutique.
Immunologie (L2)
Immunité innée et adaptative
Cytokines pro/anti-inflammatoires (TNF-α, IL-10)
MALT et IgA sécrétoire.
Expliquer la tolérance immunitaire muqueuse et les mécanismes de l'inflammation intestinale.
Biochimie (L2)
Métabolisme glucides, lipides, protéines
Structure des oligo/polysaccharides
Enzymes digestives (lactase, protéases, lipases).
Relier la structure biochimique des substrats aux mécanismes enzymatiques de dégradation par les probiotiques.
Virologie (L3)
Structure et classification des virus
Cycles lytique et lysogène des phages
Tropisme et spécificité d'hôte.
Distinguer cycle lytique et lysogène ; comprendre les implications thérapeutiques et les risques liés aux phages lysogènes.
Génétique microbienne (L3/M1)
Transfert horizontal de gènes (HGT)
Plasmides, transposons, intégrons
Notion de CRISPR-Cas9 et édition génomique.
Analyser les risques de dissémination de gènes (résistance, virulence) dans le contexte des probiotiques OGM.
Mycologie (L3)
Biologie des levures et champignons filamenteux
Métabolisme primaire/secondaire des levures
Biosécurité en mycologie.
Citer les levures à potentiel thérapeutique et leurs métabolites bioactifs ; distinguer levure probiotique et levure pathogène.
-
Opened: Thursday, 2 April 2026, 4:55 AMClosed: Monday, 6 April 2026, 4:55 AM
-
Opened: Thursday, 2 April 2026, 4:55 AMClosed: Monday, 6 April 2026, 4:55 AM
-
-
République Algérienne Démocratique et Populaire
Ministère de l'Enseignement Supérieur et de la Recherche Scientifique
Centre Universitaire Nour Bachir – El-Bayadh
Département des Sciences Biologiques

Microorganismes Thérapeutiques
Master 2 – Microbiologie Appliquée | Semestre II
Partie 1 — Introduction
Concepts fondamentaux, composition, microbiote & mécanismes
Dr. NAIMI Mostefa
Maître de Conférences A – Département des Sciences Biologiques
Année universitaire 2025–2026
Partie 1 — Introduction
1.1 Histoire, concepts et définitions
1.1.1 Jalons historiques
La notion que les microorganismes peuvent être bénéfiques pour l'hôte est ancienne. Hippocrate (env. 460–370 av. J.-C.) formulait déjà l'intuition fondatrice : « Que la nourriture soit ton médicament, et que le médicament soit ton nourriture ». La microbiologie moderne a construit progressivement ce paradigme.


Époque / Auteur
Contribution majeure
Louis Pasteur (1857)
Démonstration de la fermentation lactique par des agents vivants — fondement de la microbiologie des aliments fermentés


Époque / Auteur
Contribution majeure
Joseph Lister (1878)
Premier isolement de bactéries lactiques à partir du lait (Bacterium lactis)


Époque / Auteur
Contribution majeure
Henry Tissier (1889)
Isolement du Bifidobacterium ; corrélation entre sa présence et la santé intestinale des nourrissons.
Il a suggéré ainsi que ces bactéries pourraient être administrées aux patients souffrant de diarrhée pour aider à restaurer une flore intestinale saine.


Époque / Auteur
Contribution majeure
Élie Metchnikoff (1907)
Lien entre longévité des populations bulgares et consommation de lait fermenté ; identification de Lactobacillus bulgaricus et Streptococcus thermophilus.
Le premier à suggérer que la consommation des bactéries lactiques présentes dans ces laits fermentés pourrait avoir des effets bénéfiques sur la santé.
Prix Nobel de physiologie ou médecine (1908).


Époque / Auteur
Contribution majeure
Ernst Moro (1900)
Le premier à donner une description bactériologique de Lactobacillus acidophilus.


Époque / Auteur
Contribution majeure
Minoru Shirota (1930)
Isolement de Lactobacillus casei afin de l’utiliser pour combattre les épidémies de diarrhée et un produit utilisant cette souche a été commercialisé en 1935 (Yakult).

 Époque / Auteur
Époque / AuteurContribution majeure
Werner Kollath (1953)
Première utilisation du terme « probiotique » (du grec pro bios : pour la vie) comme antonyme d'antibiotique, pour décrire la restauration de la santé des patients souffrant de malnutrition par différents suppléments organiques et inorganiques.


Époque / Auteur
Contribution majeure
Lilly & Stillwell (1965)
Redéfinition : substances sécrétées par un microorganisme stimulant la croissance d'un autre

Époque / Auteur
Contribution majeure
Parker (1974)
Extension : organismes et substances contribuant à l'équilibre microbiologique intestinal

Époque / Auteur
Contribution majeure
Fuller (1989)
Définition classique : supplément alimentaire microbien vivant améliorant l'équilibre de la flore intestinale de l'hôte


Époque / Auteur
Contribution majeure
FAO/OMS (2001)
Définition de référence : « microorganismes vivants qui, administrés en quantités adéquates, confèrent un bénéfice pour la santé de l'hôte »



Époque / Auteur
Contribution majeure
ISAPP (2014–2021)
Consensus sur les probiotiques, prébiotiques, postbiotiques et synbiotiques — cadre conceptuel actuel


Generally Recognized as Safe “GRAS” (FDA).
Qualified Presumption of Safety “QPS” (EFSA).
Food garde & ProSafe.
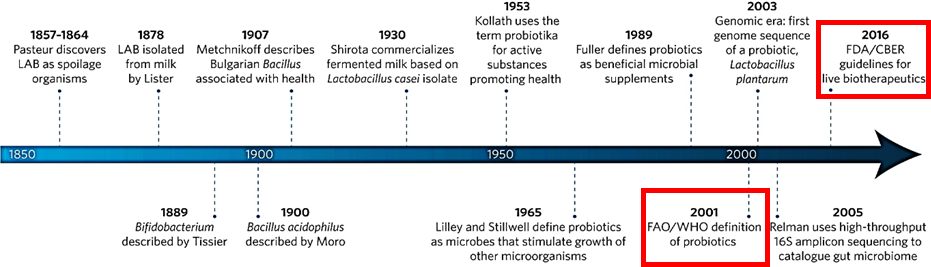
Figure N° 1.1 : Chronologie des étapes clés dans l'histoire des probiotiques et des probiotiques de nouvelle génération.
1.1.2 Définitions consensuelles actualisées (ISAPP 2014–2021)
a. Probiotique (FAO/OMS 2001 ; Hill et al., 2014)
Définition
« Microorganismes vivants qui, lorsqu'ils sont administrés en quantités adéquates, confèrent un bénéfice pour la santé de l'hôte. »
Conditions minimales : viabilité, quantité suffisante au site d'action, bénéfice documenté et spécifique à la souche.
b. Prébiotique (Gibson et al., 2017)
Définition
« Substrat utilisé sélectivement par les microorganismes de l'hôte, conférant un bénéfice pour la santé. »
Principales classes : fructo-oligosaccharides (FOS), galacto-oligosaccharides (GOS), inuline, oligosaccharides du lait maternel (OLM).
Le concept prébiotique est plus récent que celui des probiotiques et a été proposé pour la première fois en 1995 par Gibson et Roberfroid. Les aspects clés d’un prébiotique consistent dans le fait qu’il n’est pas facile à assimiler par l’hôte et qu’il confère un effet bénéfique sur la santé de l’individu en ayant une influence+ sur les microbes bénéfiques natifs.
Les prébiotiques sont des (substrats) substances alimentaires (consistant surtout en polysaccharides, à l’exclusion de l’amidon, et en oligosaccharides). La plupart des prébiotiques sont utilisés comme ingrédients alimentaires ; dans les biscuits, les céréales, le chocolat, la pâte à tartiner et les produits laitiers.
Les prébiotiques les plus communs sont :
- L’oligofructose ; se trouve naturellement dans de nombreux aliments tels le blé, les oignons, les bananes, le miel, l’ail et les poireaux. Il peut aussi être isolé à partir de la racine de la chicorée ou être synthétisé par des enzymes à partir du sucrose. Sa fermentation dans le colon engendre + effets physiologique (augmentation ; du nbre de bifidobactéries dans le côlon, de l'absorption du calcium et du poids fécal / abaissement du temps de transit gastro-intestinal et du taux de lipides sanguins).
- L’inuline ;
- Les galacto-oligosaccharides ;
- Le lactulose un disaccharide de synthèse utilisé comme médicament (constipation et de l’encéphalopathie hépatique) ;
- Les oligosaccharides du lait maternel.

Ainsi, un prébiotique peut être défini comme :
« Des ingrédients alimentaires qui influencent de façon bénéfique l’hôte en stimulant sélectivement la croissance et/ou l’activité d’un ou d’un nombre limité de groupes bactériens dans le colon et qui améliorent ainsi la santé de l’hôte ».


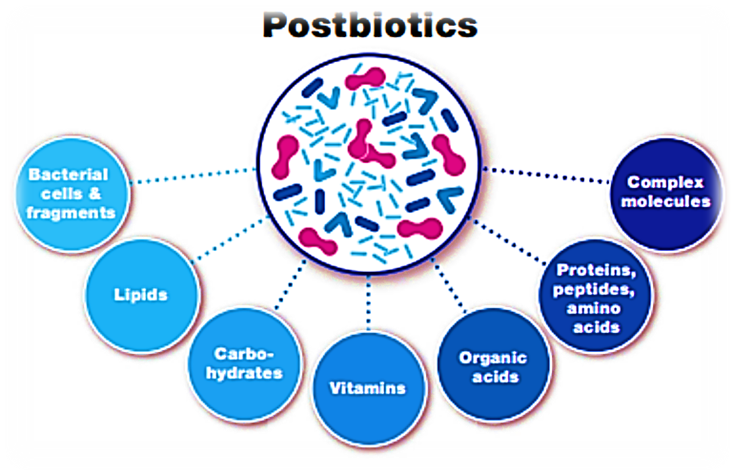
c. Postbiotique ─ Nouveau concept (Salminen et al., 2021)
Définition — Concept Actualisé
« Préparation de microorganismes inanimés et/ou de leurs composants qui confère un bénéfice pour la santé de l'hôte. »
Exemples : bactéries inactivées par la chaleur, fragments de paroi cellulaire, acides organiques, bactériocines. Avantage majeur : stabilité à température ambiante.

d. Synbiotique (Swanson et al., 2020)
Définition
« Mélange composé de microorganismes vivants et de substances alimentaires utilisées sélectivement par les microorganismes hôtes *, avec un effet bénéfique pour la santé de l’hôte. »
* Deux types : synbiotique complémentaire (prébiotique + probiotique agissant indépendamment) et synbiotique synergique (le prébiotique est le substrat spécifique du probiotique co-administré).


Les synbiotiques (terme né en 1995, sous l’impulsion de Gibson et Roberfroid) sont des combinaisons appropriées de prébiotiques et de probiotiques. Un produit synbiotique exerce un effet pré- et probiotique.

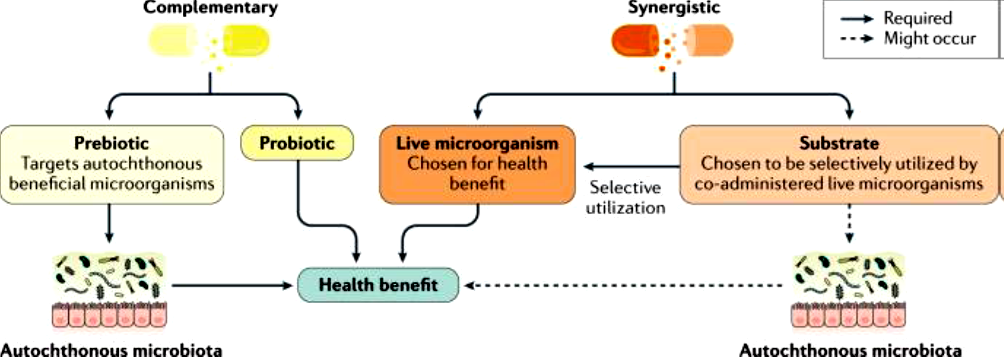
Figure N° 1.2 : Composition des symbiotiques complémentaires et synergiques. Un symbiotique complémentaire associe un prébiotique et un probiotique, lesquels agissent de manière indépendante pour induire un ou plusieurs bénéfices pour la santé. Le prébiotique fonctionne en modulant le microbiote résident afin de générer un effet bénéfique. Le symbiotique synergique est composé d'un substrat utilisé par le micro-organisme vivant co-administré, renforçant ainsi sa fonctionnalité. Les composants des symbiotiques synergiques travaillent ensemble (et non indépendamment) pour produire les bénéfices de santé qui en résultent.
Functional foods, referring to any foods or ingredients with nutritional value and that promote a health benefit to the host. Probiotics, prebiotics, and synbiotics are the most popular ingredients used as functional foods and dietary supplements.


1.1.3 Probiotiques de nouvelle génération (NGP)
Les probiotiques classiques (Lactobacillus spp., Bifidobacterium spp.) sont désormais complétés par des candidats issus de l'analyse métagénomique du microbiote humain. Ces probiotiques de nouvelle génération (Next-Generation Probiotics, NGP) ciblent des pathologies spécifiques et présentent des mécanismes d'action moléculaires caractérisés.
Tableau N° 1.1 : probiotiques de nouvelle génération (NGP), mécanismes moléculaires et applications cliniques.
Espèce NGP
Mécanisme principal
Application ciblée
Akkermansia muciniphila
Renforcement de la barrière muqueuse (Amuc_1100) ; production d'acétate et propionate ; modulation de l'immunité innée
Obésité, diabète de type 2, MICI, oncologie (checkpoint inhibiteurs)
Faecalibacterium prausnitzii
Production de butyrate ; inhibition NF-κB ; propriétés anti-inflammatoires
Maladie de Crohn, RCH, syndrome du côlon irritable
Bacteroides fragilis (souche PSA)
Production de polysaccharide A (PSA) ; induction Treg ; tolérance immunitaire
Maladies auto-immunes, inflammation intestinale
Christensenella minuta
Régulation du microbiote ; association inverse avec l'indice de masse corporelle (IMC)
Obésité, syndrome métabolique
Lachnospiraceae NK4A136
Fermentation de fibres ; production AGCC ; barrière intestinale
Prévention des infections entériques
1.2 Composition des probiotiques et critères de sélection
Les probiotiques se composent de divers types de Mos qui améliorent le microbiote intestinal. Actuellement, le groupe probiotique le plus courant est celui des bactéries lactiques, et les espèces couramment utilisées appartiennent, à des fins préventives et/ou thérapeutiques, aux genres : Lactobacillus et Bifidobacterium. Les espèces appartenant aux genres Lactococcus, Enterococcus, Carnobacterium, Streptococcus, Pediococcus, Propionibacterium, Leuconostoc, sont également considérées comme des microrganismes probiotiques.
D’autres microorganismes sont également retenus, il s’agit de Bacillus, Saccharomyces (Saccharomyces cerevisiae et Saccharomyces boulardii), Aspergillus et quelques Levures (Kluyveromyces, Pichia, Rhodotorula, Schizosaccharomyces et Candida).
1.2.1 Nomenclature mise à jour des Lactobacillaceae
En 2020, le genre Lactobacillus a été réorganisé en 23 genres distincts (Zheng et al., 2020). Cette réorganisation est désormais obligatoire dans toute publication scientifique.
Tableau N° 1.2 : Impact de la reclassification taxonomique de 2020 sur les principales souches de probiotiques et leurs cibles de santé.
Ancien nom (pré-2020)
Nouveau nom (post-2020)
Application probiotique principale
L. acidophilus
Lactobacillus acidophilus (inchangé)
Santé vaginale, digestion du lactose
L. casei
Lacticaseibacillus casei
Immunomodulation, diarrhée
L. rhamnosus
Lacticaseibacillus rhamnosus
Diarrhée du voyageur, dermatite atopique
L. plantarum
Lactiplantibacillus plantarum
MICI, syndrome du côlon irritable
L. fermentum
Limosilactobacillus fermentum
Santé vaginale, métabolisme cholestérol
L. reuteri
Limosilactobacillus reuteri
Coliques nourrissons, H. pylori
L. bulgaricus
Lactobacillus delbrueckii subsp. bulgaricus
Digestion lactose, yaourt
L. helveticus
Lactobacillus helveticus (inchangé)
Hypertension, anxiété
1.2.2 Levures et moisissures probiotiques
Tableau N° 1.3 : Caractérisation des levures et champignons filamenteux utilisés comme probiotiques ou agents enzymatiques.
Genre/Espèce
Caractéristiques
Indications
Saccharomyces cerevisiae var. boulardii
Levure non-colonisante ; résistante aux antibiotiques ; sécrète des protéases anti-toxines (C. difficile)
Diarrhée associée aux antibiotiques, infection à Clostridioides difficile, diarrhée du voyageur
Kluyveromyces marxianus
Thermotolérance élevée ; production de β-galactosidase ; GRAS
Intolérance au lactose, fromages fermentés thérapeutiques
Candida krusei (Pichia kudriavzevii)
Production de vitamine B2 ; biocontrôle ; résistance naturelle au fluconazole
Fermentations alimentaires, études de compétition microbienne
Aspergillus oryzae
Production d'enzymes digestives (protéases, amylases, lipases) ; statut GRAS FDA
Insuffisance pancréatique exocrine, aide à la digestion
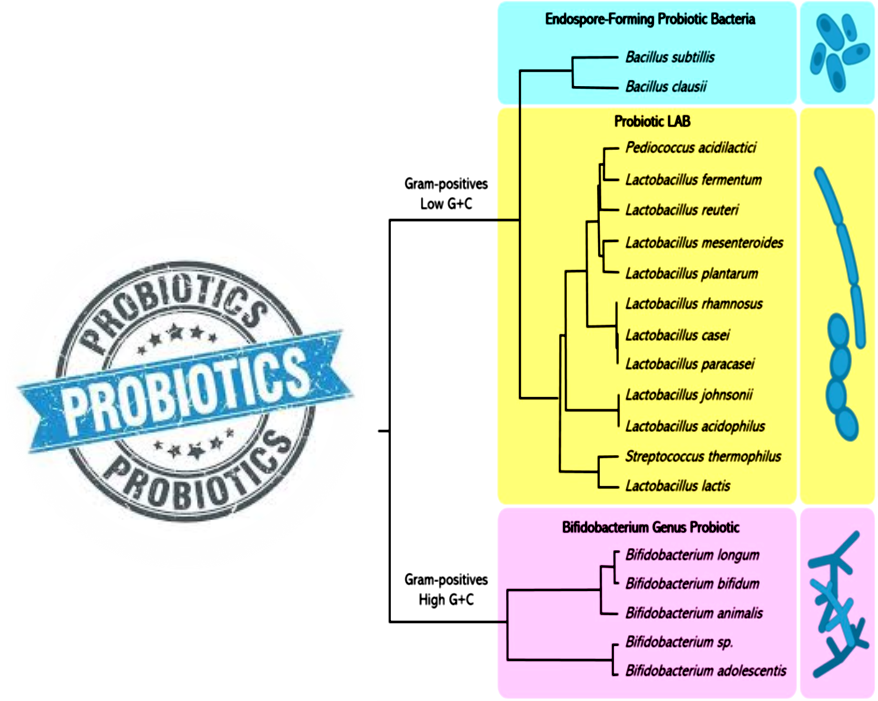
Figure N° 1.3 : Arbre phylogénétique des différents groupes bactériens probiotiques.
Les catégories de des produits à usage humain contenant micrrorganismes vivants, comprennent désormais au moins quatre, à savoir :
(1) Les aliments et compléments alimentaires ;
(2) Les cosmétiques ;
(3) Les aliments médicaux (alicaments) et
(4) les médicaments “live biotherapeutic products”(LBPs).
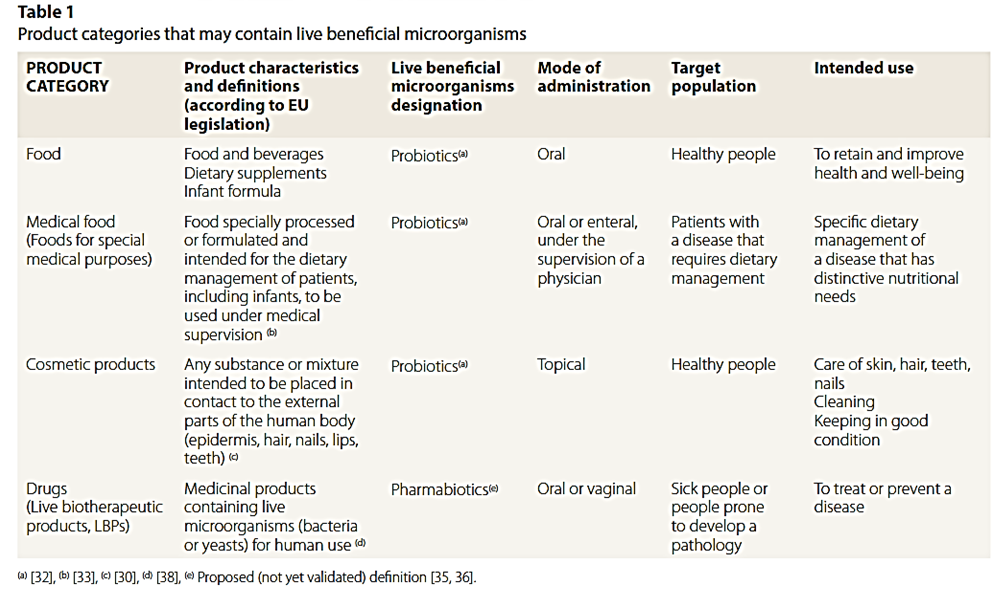
1.2.3 Critères de sélection des probiotiques
La sélection d'un microorganisme probiotique repose sur une évaluation multi-niveaux couvrant la sécurité, la fonctionnalité et les propriétés technologiques.
Tableau N° 1.4 : Critères clés et souhaitables de sélection des probiotiques (FAO/OMS, 2002).
Critères De Sécurité (obligatoires)
• Identification précise au niveau de la souche (séquençage du génome complet recommandé)
• Statut QPS (Qualified Presumption of Safety – EFSA) ou GRAS (FDA)
• Absence de facteurs de virulence (gènes de toxines, adhésines pathogènes)
• Profil de résistance aux antibiotiques : absence de résistances transmissibles (plasmides, transposons)
• Tolérance par l'hôte immunodéprimé documentée
Critères Fonctionnels (essentiels)
• Survie au pH gastrique (pH 2–3) pendant 3 heures minimum
• Résistance à la bile (0,3–0,5 % de sels biliaires) pendant 4 heures minimum
• Capacité d'adhésion à l'épithélium intestinal (lignée Caco-2, HT-29)
• Production de substances antimicrobiennes (bactériocines, acide lactique, H₂O₂, reuterine)
• Exclusion compétitive des agents pathogènes
• Immunomodulation documentée (stimulation IgA sécrétoire, équilibre Th1/Th2/Treg)
• Activité sur l'hôte spécifiquement démontrée (essais cliniques contrôlés randomisés)
Critères Technologiques (pour application alimentaire)
• Viabilité ≥ 10⁶ à 10⁷ UFC/g ou mL au moment de la consommation
• Stabilité en cours de production, transport et stockage
• Compatibilité avec les matrices alimentaires (lait, fromage, boissons)
• Tolérance aux procédés technologiques (pasteurisation douce, lyophilisation)
• Caractéristiques organoleptiques acceptables
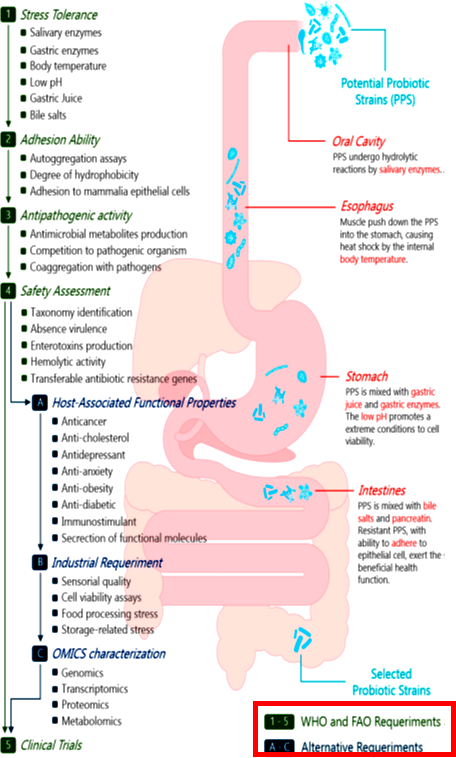
Figure N° 1.4 : Approche systématique de criblage et évaluation protectifs, fonctionnels et technologiques requis selon les lignes directrices de la FAO/OMS, (2002) et autres études (de Melo Pereira et al., 2018).
1.3 Microflore du système digestif
1.3.1 Composition et répartition du microbiote intestinal
Le système digestif constitue la plus grande interface avec l'environnement extérieur (agents exogènes : virus, bactéries, etc.) et le principal réservoir de microorganismes du corps humain.
Le système digestif du fœtus est stérile, mais a la naissance ou peu après, il acquiert rapidement un microbiote caractéristique (colonisation) par contact avec la mère (transmission verticale maternelle) et l‘environnement.
Avec le temps, une population microbienne à évolution dynamique, très complexe mais en équilibre (eubiose), non homogène constituée de 101 à 103 bactéries/g de contenu dans l'estomac et le duodénum, progressant jusqu'à 104 à 107 bactéries/g dans le jéjunum et l'iléon et culminant à 1011-1012, jusqu'à 1014, bactéries/g dans le côlon, incluant environ 500-1000 types (ou plus de 1000) de différentes espèces, s'établit de façon stable.
Ceux-ci incluent Bacteroides, Lactobacillus, Clostridium, Fusobacterium, Bifidobacterium, Eubacterium, Peptococcus, Peptostreptococcus, Escherichia et Veillonella.
Ces derniers appartiennent à 4 grands groupes phylogénétiques, à savoir : Actinobacteria, Bacteroidetes, Firmicutes et Protebacteria.
Il a été estimé que le microbiote intestinal constitue 35 à 50 % du volume du côlon humain et qu’il correspond environ aux 2 tiers du microbiote humain total.
Dans ce microenvironnement complexe il existe plusieurs modes d'interaction entre micro-organismes/l‘organisme hôte, ainsi qu'entre eux.
Ce microbiote presque commun, essentiellement la composition dominante, est stable au fil du temps, dès l’âge d’un an à l’âge adulte.
Cependant, il existe de nombreux facteurs, endogènes ou exogènes, susceptibles d'influencer sa composition, tels que :
- Le génotype de l’hôte ;
- Le mode d'accouchement et le mode d’alitement ;
- La physiologie et physicochimie de tube digestif ;
- L'âge, le stress, l’hygiène excessive, les facteurs géographiques et culturels, les thérapies surtout par usage des antibiotiques ;
- La diète (régime alimentaire et également l’ingestion de d'autres micro-organismes comme les probiotiques). Les bactéries lactiques constituent une partie intégrante de ce microbiote.
Le microbiote intestinal humain constitue l'ensemble des microorganismes résidant dans le tube digestif. Sa caractérisation a été révolutionnée par le séquençage métagénomique de l'ARNr 16S et les approches métagénomique shotgun. Les données actualisées du projet MetaHIT et du Human Microbiome Project permettent une description plus précise que les estimations antérieures.
Tableau N° 1.5 : Caractéristiques écologiques du tractus gastro-intestinal : de la densité bactérienne à la dominance des phyla.
Segment
Densité (UFC/g)
Phyla dominants
pH approximatif
Estomac
< 10³
Helicobacteraceae, Lactobacillaceae
1,5 – 3,5
Duodénum
10¹ – 10³
Streptococcaceae, Lactobacillaceae
6,0 – 7,0
Jéjunum / Iléon proximal
10⁴ – 10⁷
Lactobacillaceae, Enterococcaceae
6,5 – 7,5
Iléon terminal
10⁷ – 10⁹
Lachnospiraceae, Ruminococcaceae
7,0 – 7,5
Côlon
10¹⁰ – 10¹²
Firmicutes, Bacteroidota, Actinobacteria
5,5 – 7,0
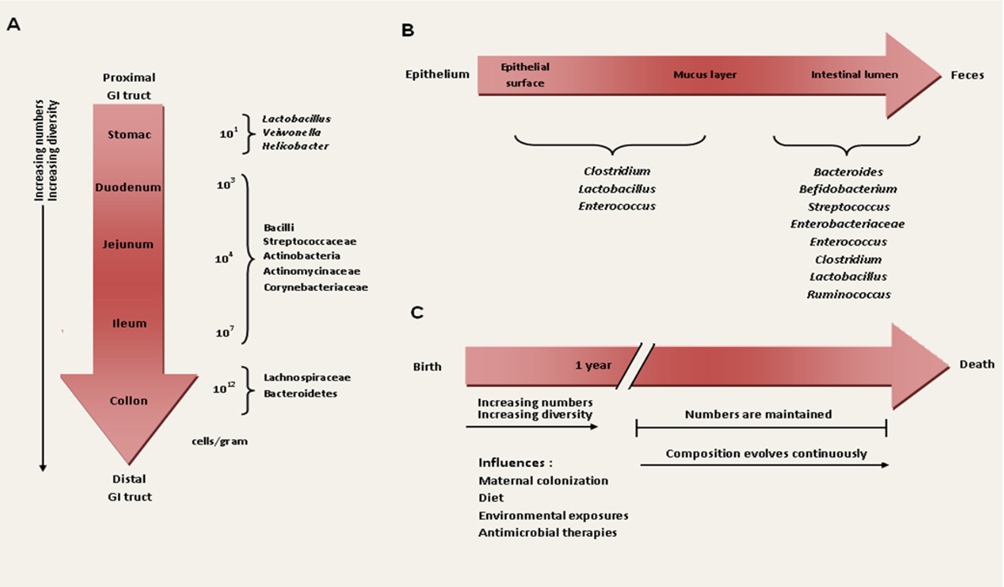
Figure N° 1.5 : Aspects spatiaux et temporels de la composition du microbiote intestinal. (a) : variations du nombre et de la composition des microbes sur toute la longueur du tractus gastro-intestinal. (b) : variations longitudinales de la composition microbienne dans l'intestin. (c) : aspects temporels de l'établissement et du maintien du microbiote, et facteurs influençant la composition microbienne.
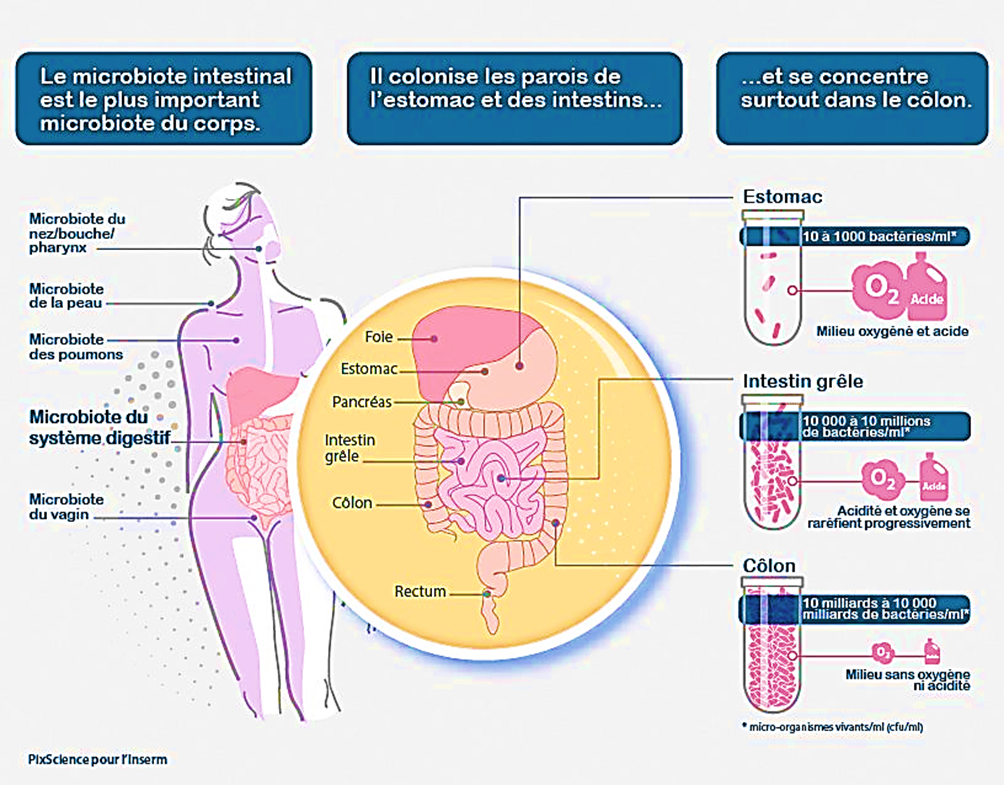
Figure N° 1.5 : Microbiote intestinal.
1.3.2 Axe intestin-cerveau (gut-brain axis)
L'axe intestin-cerveau constitue une voie de communication bidirectionnelle entre le microbiote intestinal et le système nerveux central. Il implique plusieurs relais :
• Voie neurale : nerf vague (80 % de fibres afférentes) → noyau du tractus solitaire
• Voie endocrinienne : cellules entéro-endocrines → sérotonine (95 % de la sérotonine corporelle est intestinale), GLP-1, PYY
• Voie immunitaire : cytokines inflammatoires (IL-6, TNF-α, IL-10) circulantes
• Voie métabolique : acides gras à chaîne courte (AGCC) → traversent la barrière hémato-encéphalique
Applications cliniques des probiotiques ciblant l'axe intestin-cerveau : dépression, anxiété, troubles du spectre autistique, maladie de Parkinson (accumulation d'α-synucléine initiée dans l'intestin — hypothèse de Braak).
1.3.3 Eubiose, dysbiose et implications thérapeutiques
EUBIOSE vs DYSBIOSE
Eubiose : état d'équilibre du microbiote caractérisé par une diversité α élevée (indice Shannon > 3), une dominance de Firmicutes et Bacteroidota, et une abondance en producteurs de butyrate (Faecalibacterium prausnitzii, Roseburia spp.).
Dysbiose : déséquilibre quantitatif et/ou qualitatif du microbiote associé à de nombreuses pathologies : MICI, syndrome métabolique, obésité, diabète de type 2, allergies, troubles neuropsychiatriques, cancer colorectal.
Principales causes de dysbiose : antibiothérapie, alimentation ultra-transformée, stress chronique, mode de naissance (césarienne), absence d'allaitement maternel.
1.4 Mécanismes de probiose
1.4.1 Définition et concept
La probiose (probiosis) désigne une association interspécifique bénéfique, dans laquelle l'activité d'un microorganisme améliore la santé ou les processus vitaux d'un autre organisme ou de l'hôte. Elle s'oppose à l'antibiose. Dans un contexte clinique, la probiose décrit l'ensemble des mécanismes par lesquels les microorganismes probiotiques exercent leurs effets bénéfiques sur l'hôte.

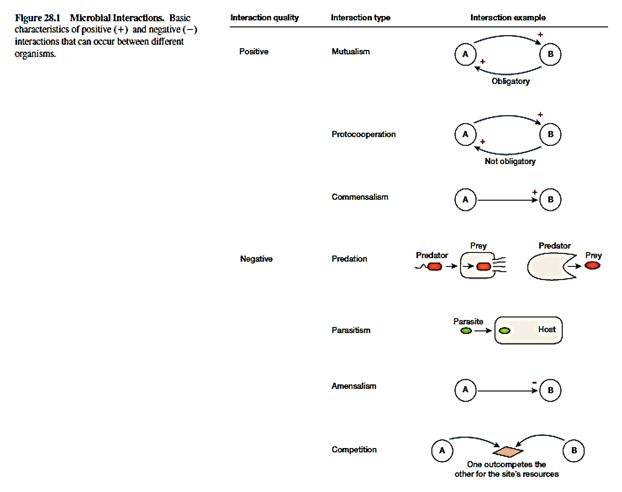
Figure N° 1.6 : Synthèse des interactions microbiennes : (a) positive & négative, (b)types ; mutualisme, commensalisme, prédation, etc..
1.4.2 Mécanismes directs
Les probiotiques exercent leurs effets par plusieurs mécanismes directs agissant au sein de la lumière intestinale :
• Exclusion compétitive : occupation des sites de liaison épithéliaux, empêchant l'adhésion des pathogènes
• Production de substances antimicrobiennes :
– Bactériocines (nisine, lactocine, plantaricine) — spectre d'action variable
– Acide lactique et acide acétique — abaissement du pH luminal
– Peroxyde d'hydrogène (H₂O₂) — activité bactériostatique en milieu aérobie
– Reuterine (3-hydroxypropionaldéhyde) — large spectre antimicrobien (Limosilactobacillus reuteri)
• Compétition nutritionnelle : consommation des substrats nécessaires à la croissance des pathogènes
• Co-agrégation : formation d'agrégats avec les pathogènes facilitant leur élimination
1.4.3 Mécanismes indirects — Renforcement de la barrière intestinale
• Stimulation de la production de mucus (cellules caliciformes) — couche de gel protectrice
• Consolidation des jonctions serrées (tight junctions) : surexpression des claudines, occludines, ZO-1
• Induction de la production d'IgA sécrétoire (sIgA) — première ligne de défense humorale muqueuse
• Stimulation des cellules de Paneth → production de défensines (peptides antimicrobiens)
1.4.4 Mécanismes immunologiques
L'interaction entre les probiotiques et le système immunitaire intestinal est médiée par plusieurs récepteurs de reconnaissance de motifs (PRR) :
• TLR (Toll-Like Receptors) : TLR2 reconnaît les acides lipotéichoïques (Gram+) ; TLR4 reconnaît le LPS (Gram-)
• NOD1/NOD2 : détection intracellulaire des fragments de peptidoglycane
• Effets immunologiques résultants :
– Polarisation Th1/Th2/Th17/Treg selon la souche et la dose
– Augmentation de l'IL-10 et du TGF-β (cytokines anti-inflammatoires)
– Induction de cellules dendritiques tolérogènes
– Amplification de la production d'IgA sécrétoire
1.4.5 Effets métaboliques — Production d'AGCC
La fermentation des fibres prébiotiques par les bactéries probiotiques génère des acides gras à chaîne courte (AGCC), principalement :
• Butyrate (C4) : source énergétique des colonocytes (70 % de l'énergie) ; propriétés anti-inflammatoires ; inhibition des histones déacétylases (HDAC)
• Propionate (C3) : absorption hépatique ; régulation de la néoglucogenèse ; signal de satiété
• Acétate (C2) : le plus abondant ; absorbé dans la circulation périphérique ; précurseur du cholestérol
Rôle des AGCC au-delà de l'intestin : récepteurs GPR41, GPR43 sur les cellules immunitaires, adipocytes et neurones entériques — lien direct avec l'axe intestin-cerveau.


Références bibliographiques
Cryan J.F. et al. (2019). The Microbiota-Gut-Brain Axis. Physiological Reviews, 99(4), 1877–2013. https://doi.org/10.1152/physrev.00018.2018
Gibson G.R. et al. (2017). Expert consensus document: The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of prebiotics. Nature Reviews Gastroenterology & Hepatology, 14(8), 491–502. https://doi.org/10.1038/nrgastro.2017.75
Hill C. et al. (2014). Expert consensus document. The International Scientific Association for Probiotics and Prebiotics consensus statement on the scope and appropriate use of the term probiotic. Nature Reviews Microbiology, 12(8), 506–514. https://doi.org/10.1038/nrgastro.2014.66
Journal Officiel de la République Algérienne — Décret exécutif n° 23-106 relatif aux compléments alimentaires : dispositions applicables aux produits contenant des microorganismes vivants.
Lopez-Siles M. et al. (2017). Faecalibacterium prausnitzii: from microbiology to diagnostics and prognostics. ISME Journal, 11(4), 841–852. https://doi.org/10.1038/ismej.2016.176
Plovier H. et al. (2017). A purified membrane protein from Akkermansia muciniphila or the pasteurized bacterium improves metabolism in obese and diabetic mice. Nature Medicine, 23(1), 107-113. https://doi.org/10.1038/nm.4236
Salminen S. et al. (2021). The International Scientific Association of Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of postbiotics. Nature Reviews Gastroenterology & Hepatology, 18(9), 649-667. https://doi.org/10.1038/s41575-021-00440-6
Shreiner A.B. et al. (2015). The gut microbiome in health and in disease. Current Opinion in Gastroenterology, 31(1), 69-75. https://doi.org/10.1097/MOG.0000000000000139
Swanson K.S. et al. (2020). The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of synbiotics. Nature Reviews Gastroenterology & Hepatology, 17(11), 687-701. https://doi.org/10.1038/s41575-020-0344-2
Wastyk H.C. et al. (2021). Gut-microbiota-targeted diets modulate human immune status. Cell, 184(16), 4137-4153. https://doi.org/10.1016/j.cell.2021.06.019*
Zheng J. et al. (2020). A taxonomic note on the genus Lactobacillus: Description of 23 novel genera, emended description of the genus Lactobacillus Beijerinck 1901, and union of Lactobacillaceae and Leuconostocaceae. International Journal of Systematic and Evolutionary Microbiology, 70(4), 2782-2858. https://doi.org/10.1099/ijsem.0.004107
-
<
République Algérienne Démocratique et Populaire
Ministère de l'Enseignement Supérieur et de la Recherche Scientifique
Centre Universitaire Nour Bachir – El-Bayadh
Département des Sciences Biologiques
Microorganismes Thérapeutiques
Master 2 – Microbiologie Appliquée | Semestre II
Partie 2 — Effets sur le métabolisme de l'hôte
Métabolisme, immunité, détoxification, activité anticarcinogénique & mécanismes d'action
Dr. NAIMI Mostefa
Maître de Conférences A – Département des Sciences Biologiques
Année universitaire 2025–2026
Partie 2 — Effets sur le métabolısme de l'hôte
Une grande variété d’effets bénéfiques potentiels sur la santé ont été attribués aux probiotiques, allant de soulagement des diarrhées et de la constipation, soulagement de la mauvaise digestion du lactose, à la prévention de maladies graves potentiellement mortelles telles que les maladies inflammatoires de l'intestin, le cancer et les incidents cardiovasculaires (l'effet sur le taux de cholestérol sanguin).
2.1 Renforcement du métabolisme
2.1.1 Production de vitamines et cofacteurs
Les microorganismes probiotiques contribuent significativement à la biosynthèse de vitamines essentielles dans le côlon, suppléant partiellement aux apports alimentaires :
a. Vitamines du groupe B
– Vitamine B2 (riboflavine) : produite par Lacticaseibacillus fermentum, L. plantarum ; rôle dans le métabolisme énergétique (FAD, FMN)
– Vitamine B9 (acide folique) : synthétisée par Bifidobacterium spp. et certains Lactobacillaceae ; indispensable à la synthèse des bases nucléiques
– Vitamine B12 (cobalamine) : produite par Propionibacterium freudenreichii et Lactobacillus reuteri ; essentielle à l'hématopoïèse et à la myélinisation
– Vitamine B7 (biotine) : synthétisée par Bifidobacterium spp. ; cofacteur des carboxylases.
b. Vitamine K2 (ménaquinone) : produite principalement par Bacillus subtilis natto (nattō japonais) et certains Lactobacillaceae ; rôle dans la coagulation sanguine et le métabolisme osseux (carboxylation de l'ostéocalcine)
c. Acides aminés essentiels : production de lysine, tryptophane (précurseur de la sérotonine) et méthionine par certains Lactobacillaceae en conditions de déficience alimentaire.
2.1.2 Production d'enzymes digestives
• β-galactosidase (lactase) : hydrolyse le lactose en glucose + galactose → soulagement de l'intolérance au lactose
• Protéases : hydrolyse partielle des protéines alimentaires → amélioration de la digestibilité, réduction de l'allergenicité (caséines, gluten)
• Lipases : hydrolyse des triglycérides → amélioration de l'absorption des acides gras à chaîne longue
• Phytases : hydrolyse de l'acide phytique → amélioration de la biodisponibilité des minéraux (Fe²⁺, Zn²⁺, Ca²⁺, Mg²⁺)
• Amylases (Bacillus, Aspergillus oryzae) : digestion de l'amidon résistant → production d'AGCC
2.1.3 Acides gras à chaîne courte (AGCC)
La production d'AGCC par fermentation microbienne des fibres prébiotiques représente l'un des mécanismes les plus importants de l'action métabolique des probiotiques.
AGCC
Producteurs principaux
Mécanismes d'action
Effets systémiques
Butyrate (C4)
Faecalibacterium prausnitzii, Roseburia spp., Butyrivibrio fibrisolvens
Énergie colonocytes (70%) ; inhibition HDAC ; activation GPR109A ; induction Treg coliques
Anti-inflammatoire ; préventif cancer colorectal ; amélioration barrière intestinale
Propionate (C3)
Bacteroides spp., Akkermansia muciniphila, Veillonella spp.
Inhibition synthèse hépatique du cholestérol ; stimulation PYY et GLP-1 (satiété) ; activation GPR41/43
Réduction cholestérolémie ; régulation glycémique ; signal de satiété
Acétate (C2)
Bifidobacterium spp., Lactobacillaceae
Substrat du métabolisme périphérique ; précurseur lipides ; activation GPR43 sur cellules immunitaires
Source énergétique cérébrale ; régulation appétit ; modulation réponse immunitaire
2.2 Stimulation du système immunitaire
2.2.1 Immunomodulation intestinale
L'interaction probiotiques–système immunitaire est médiée par des récepteurs de reconnaissance de motifs (PRR) exprimés sur les cellules épithéliales intestinales (IEC), les cellules dendritiques (DC) et les macrophages de la lamina propria :
• Voie TLR2 (acides lipotéichoïques, peptidoglycane Gram+) → activation NF-κB modérée → production IL-10, TGF-β (profil anti-inflammatoire).
• Voie TLR4 (LPS de Gram-) → selon la souche : tolérance ou activation immunitaire
• Voie NOD2 (muramyl dipeptide) → activation inflammasome NLR → contrôle de l'inflammation.
• Signalisation DC → polarisation Th1/Th2/Th17/Treg selon la nature du probiotique.
2.2.2 Effets immunologiques
Effets immunitaires clés des probiotiques
• Augmentation de l'IgA sécrétoire (sIgA) : première ligne de défense humorale muqueuse — neutralisation des pathogènes luminaux
• Induction des Treg (cellules T régulatrices CD4+CD25+FoxP3+) : production IL-10 et TGF-β → tolérance immunitaire, prévention allergie et MICI
• Équilibre Th1/Th2 : correction du déséquilibre Th2 dans les allergies atopiques par stimulation Th1 (Bifidobacterium longum, L. acidophilus)
• Stimulation NK (Natural Killer cells) : renforcement de la surveillance anti-tumorale (Lacticaseibacillus rhamnosus GG)
• Réduction des cytokines pro-inflammatoires (TNF-α, IL-6, IL-1β) dans les MICI et le syndrome du côlon irritable
• Activation des macrophages M2 (profil anti-inflammatoire) : phagocytose, résolution de l'inflammation
2.2.3 Probiotiques et maladies inflammatoires chroniques de l'intestin (MICI)
Les MICI (maladie de Crohn et rectocolite hémorragique) sont caractérisées par une dysbiose profonde (réduction de F. prausnitzii, augmentation d'E. coli adhérent-invasif) et une activation immunitaire muqueuse inappropriée. L'utilisation de probiotiques dans les MICI repose sur plusieurs mécanismes :
• Rétablissement de la diversité microbienne (indice Shannon).
• Réduction de l'inflammation muqueuse via induction Treg.
• Renforcement des jonctions serrées (ZO-1, claudines) — réduction de la perméabilité intestinale.
• Efficacité clinique documentée : Escherichia coli Nissle 1917 (Mutaflor®) = équivalent mésalazine pour maintien de rémission dans la RCH (Rembacken et al., Lancet, 1999).
2.3 Probiotiques et intolérance au lactose
L'intolérance au lactose affecte environ 65 % de la population mondiale adulte (prévalence plus élevée en Afrique du Nord et en Asie). Elle résulte d'une déficience en lactase (β-D-galactosidase) intestinale entraînant la fermentation colique du lactose non-digéré par les bactéries intestinales, génératrice de gaz (H₂, CO₂, CH₄) et d'acides organiques responsables des symptômes digestifs.
2.3.1 Mécanismes d'action probiotiques
• Apport exogène de β-galactosidase microbienne : Lacticaseibacillus bulgaricus et Streptococcus thermophilus (dans le yaourt) produisent une β-galactosidase active in situ dans l'intestin grêle
• Libération de la β-galactosidase lors de la lyse bactérienne dans la lumière intestinale.
• Ralentissement du transit intestinal par les bactéries vivantes → augmentation du temps de contact lactase–lactose.
• Adaptation du microbiote colique : induction de la production de β-galactosidase par les bactéries résidentes.
2.3.2 Données cliniques actualisées
Une méta-analyse récente (Savaiano & Hutkins, 2021) confirme que la consommation de yaourt contenant des cultures vivantes de S. thermophilus et L. bulgaricus réduit significativement les symptômes d'intolérance au lactose par rapport au lait non fermenté, indépendamment de la dose de lactose.
L'EFSA (Autorité Européenne de Sécurité des Aliments) a validé l'allégation de santé : « Les cultures de yaourt vivantes améliorent la digestion du lactose chez les individus présentant une maldigestion du lactose » (EFSA, 2010).
2.4 Détoxification
Les microorganismes probiotiques participent activement à la détoxification de l'organisme par plusieurs mécanismes directs et indirects :
2.4.1 Dégradation des facteurs antinutritionnels
• Phytates (acide phytique) : dégradation par les phytases bactériennes → libération des minéraux chélatés (Fe²⁺, Zn²⁺, Ca²⁺).
• Glucosinolates (choux, crucifères) : dégradation par les bactéries du microbiote → réduction de la goitrogenicité.
• Oxalates : dégradation par Oxalobacter formigenes et certains Lactobacillaceae → prévention des lithiases rénales oxalocalciques.
• Tanins et polyphénols : biotransformation par le microbiote → production de métabolites bioactifs (urolithines, équol).
2.4.2 Inhibition des microorganismes toxinogènes
• Compétition nutritionnelle et exclusion compétitive des bactéries productrices de toxines (Clostridium difficile, C. perfringens, E. coli entérotoxinogène).
• Acidification du milieu intestinal → inhibition des enzymes de décarboxylation bactériennes responsables de la production d'amines biogènes (histamine, tyramine, putrescine).
• Production de bactériocines → inhibition de C. difficile (S. boulardii produit des protéases neutralisant les toxines A et B).
2.4.3 Liaison des mycotoxines et métaux lourds
Des données récentes (Haskard et al. ; Assaf et al., 2019) montrent la capacité de certains Lactobacillaceae à lier par adsorption physique sur leur paroi cellulaire (peptidoglycane, acides teichoïques) :
• Aflatoxine B1 (AF B1) : liée par Lactobacillus acidophilus et Bifidobacterium longum — réduction de la biodisponibilité.
• Ochratoxine A : adsorption par les parois de levures (S. cerevisiae var. boulardii)
• Plomb (Pb²⁺) et cadmium (Cd²⁺) : chélation par les groupements carboxylates et phosphates des biopolymères bactériens.
2.5 Activité anticarcinogénique
2.5.1 Mécanismes anticarcinogènes des probiotiques
Des données précliniques et cliniques croissantes soutiennent un rôle des probiotiques dans la prévention et le traitement adjuvant de certains cancers. Les mécanismes impliqués sont multiples et interdépendants :
Mécanismes anticarcinogènes directs
• Inhibition de la croissance des cellules tumorales : production de butyrate → inhibition HDAC → induction de l'apoptose et différenciation cellulaire
• Stimulation immunitaire anti-tumorale : activation des cellules NK et des lymphocytes T cytotoxiques CD8+ → surveillance anti-tumorale
• Suppression des bactéries pro-cancérogènes productrices de β-glucosidase, β-glucuronidase, azoréductase → réduction de la libération de carcinogènes à partir de complexes inoffensifs
• Destruction des nitrosamines et suppression des nitroréductases → réduction de la synthèse endogène de N-nitrosamines à partir des nitrites alimentaires
Mécanismes anticarcinogènes indirects
• Réduction de la perméabilité intestinale → diminution de l'exposition aux carcinogènes luminaux
• Modulation du métabolisme des acides biliaires secondaires (désoxycholique, lithocholique) — agents promoteurs de cancer colorectal
• Maintien de l'eubiose → réduction de l'activation des pro-carcinogènes par les enzymes bactériennes
• Production d'acide linoléique conjugué (CLA) par Lacticaseibacillus rhamnosus et certains Propionibacterium spp. → propriétés antiprolifératives documentées
2.5.2 Probiotiques et immunothérapie anticancéreuse
Une avancée majeure des années 2020 : plusieurs études ont établi un lien entre la composition du microbiote intestinal et la réponse aux inhibiteurs de points de contrôle immunitaire (checkpoint inhibitors : anti-PD-1, anti-CTLA-4).
• Akkermansia muciniphila et Faecalibacterium prausnitzii sont associés à une meilleure réponse à l'immunothérapie anti-PD-1 dans les mélanomes et cancers du poumon (Routy et al., 2018 ; Gopalakrishnan et al., 2018).
• Mécanisme proposé : augmentation de l'infiltration tumorale par les lymphocytes T CD8+ via modulation des DC intestinales.
• Essais cliniques en cours : supplémentation en A. muciniphila pasteurisée en adjuvant de l'immunothérapie (NCT03865212).
• Implication pratique : l'utilisation d'antibiotiques avant immunothérapie dégrade le microbiote et réduit l'efficacité du traitement → recommandation de préserver le microbiote.
2.5.3 Cancers spécifiques et probiotiques
Type de cancer
Microorganisme probiotique
Mécanisme principal
Niveau de preuve
Cancer colorectal
Lacticaseibacillus rhamnosus GG, Bifidobacterium longum, F. prausnitzii
Butyrate → apoptose ; suppression β-glucuronidase ; immunité anti-tumorale
Préclinique fort / Clinique modéré
Cancer du sein
Lactobacillus acidophilus, Bif. lactis
Modulation estrogènes ; production CLA ; immunostimulation
Préclinique modéré
Cancer de la vessie
Mycobacterium bovis (BCG)
Activation immunitaire locale (macrophages, NK, lymphocytes T)
Clinique fort (standard de soin)
Mélanome / CBNPC
Akkermansia muciniphila
Potentialisation de l'immunothérapie anti-PD-1
Clinique émergent (essais de phase II)
2.6 Autres effets thérapeutiques
2.6.1 Maladies cardiovasculaires — Réduction du cholestérol
L'hypercholestérolémie constitue un facteur de risque cardiovasculaire majeur. Plusieurs mécanismes probiotiques contribuent à la réduction du cholestérol plasmatique :
• Assimilation intracellulaire du cholestérol par les bactéries lactiques en phase de croissance.
• Déconjugaison des acides biliaires par les hydrolases des sels biliaires (BSH) bactériennes → élimination fécale accrue des acides biliaires → augmentation de la synthèse hépatique d'acides biliaires à partir du cholestérol.
• Liaison du cholestérol aux parois cellulaires bactériennes (groupements peptidoglycane)
• Réduction de la synthèse hépatique du cholestérol par le propionate (inhibition HMG-CoA réductase).
Méta-analyse (Wu et al., 2017) : réduction moyenne du LDL-cholestérol de 8,7 mg/dL et du cholestérol total de 8,4 mg/dL avec la supplémentation probiotique.
2.6.2 Diabète de type 2 et syndrome métabolique
• Amélioration de la sensibilité à l'insuline : réduction de l'inflammation systémique de bas grade (LPS-LBP axis).
• Réduction de l'endotoxémie métabolique : le butyrate renforce la barrière intestinale → réduction du passage de LPS dans la circulation.
• GLP-1 et PYY : stimulés par le propionate → amélioration de la sécrétion d'insuline en réponse au glucose.
• A. muciniphila : administration de la bactérie pasteurisée → amélioration de la sensibilité à l'insuline dans un essai clinique de Phase I/II (Plovier et al., 2017 ; Depommier et al., 2019).
2.6.3 Santé mentale — Psychobiotiques
Le terme psychobiotique (Dinan et al., 2013) désigne tout probiotique exerçant un effet bénéfique sur la santé mentale via l'axe intestin-cerveau.
• Lacticaseibacillus rhamnosus JB-1 : réduction de l'anxiété et du comportement dépressif chez l'animal via le nerf vague ; réduction du cortisol chez l'humain.
• Bifidobacterium longum NCC3001 : réduction de la dépression dans le SCI (Pinto-Sanchez et al., 2017).
• Formulations multi-souches : réduction de la rumination et des pensées agressives (Steenbergen et al., 2015).
• Mécanismes impliqués : production de GABA, sérotonine précurseurs ; modulation de l'axe HPA (hypothalamo-hypophyso-surrénalien) ; réduction de l'inflammation neuroinflammation.
2.6.4 Prévention/traitement des infections
Helicobacter pylori (Gram–, spiralé, uréase+) : agent étiologique des gastrites chroniques, ulcères gastroduodénaux et cancer gastrique (carcinogène de groupe I, CIRC).
• Mécanismes anti-H. pylori des probiotiques : compétition pour les récepteurs de Lewis (b) de l'épithélium gastrique ; production de bactériocines (L. acidophilus, L. reuteri) ; inhibition de l'uréase ; réduction de l'inflammation gastrique.
• Application clinique : co-administration de probiotiques (L. reuteri DSM 17938) lors de la trithérapie anti-H. pylori → réduction des effets secondaires (diarrhée) de 50 % et amélioration du taux d'éradication (Zhang et al., 2020).
COVID-19 et microbiote (données 2021–2023) : patients COVID-19 présentent une dysbiose sévère (réduction de Bifidobacterium, augmentation d'Enterobacteriaceae) corrélée à la sévérité clinique. Des essais cliniques explorent l'utilisation de probiotiques multi-souches pour réduire la sévérité du COVID long (Gut, 2021).
2.7 Mécanismes d'action des probiotiques dans l'intestin
Trois niveaux d'action intégrés résument l'ensemble des mécanismes des probiotiques :
Niveau 1 — Interactions microbiennes luminales
• Exclusion compétitive des pathogènes (sites d'adhésion, nutriments)
• Production de substances antimicrobiennes (bactériocines, acides organiques, H₂O₂)
• Co-agrégation et formation de biofilms bénéfiques
• Modulation du pH luminal
Niveau 2 — Renforcement de la barrière muqueuse
• Stimulation de la production de mucus (MUC2, MUC3) par les cellules caliciformes
• Consolidation des jonctions serrées (ZO-1, claudines 1/3/4, occludine)
• Induction de la production de défensines et cathelicidines par les cellules de Paneth
• Stimulation de la réparation épithéliale (EGF, prolifération colonocytaire)
Niveau 3 — Immunomodulation systémique et métabolique
• Dialogue avec les cellules dendritiques et les macrophages sous-épithéliaux
• Induction des lymphocytes Treg → tolérance immunitaire
• Production d'AGCC → effets systémiques (cerveau, foie, adipose, système immunitaire)
• Modulation de l'axe intestin-cerveau (via nerf vague, sérotonine, GABA)
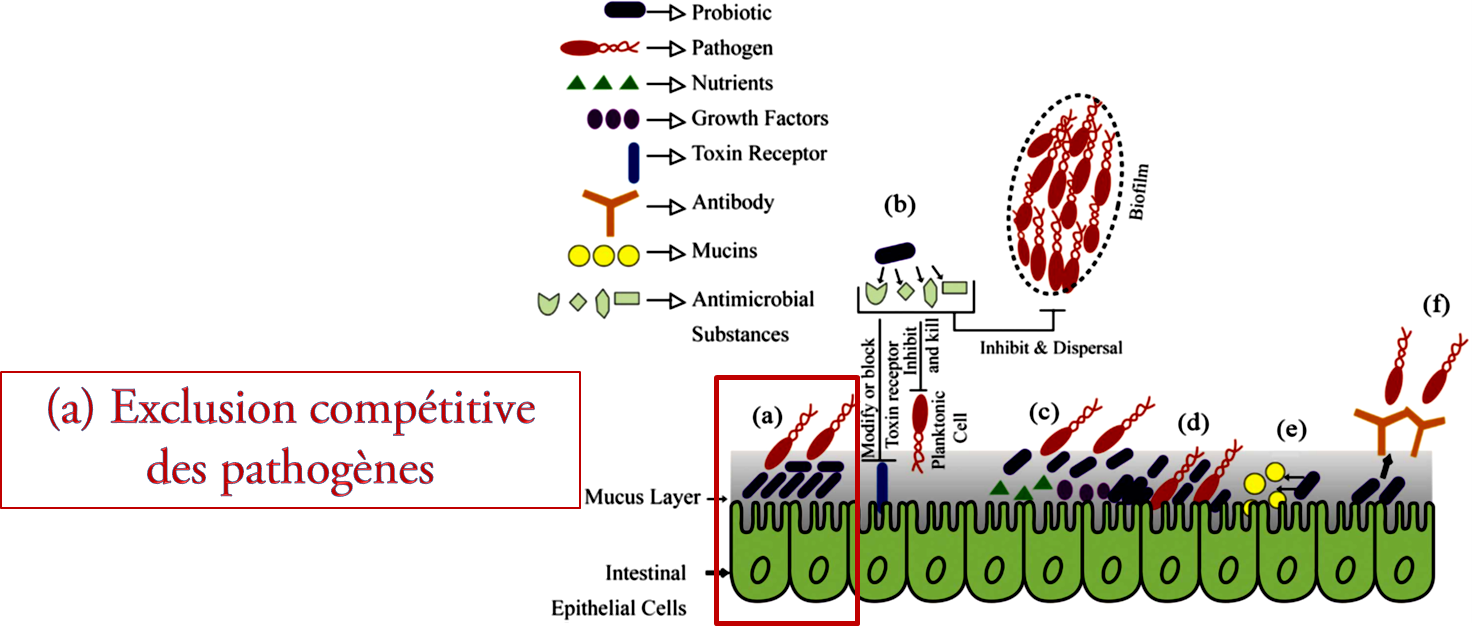
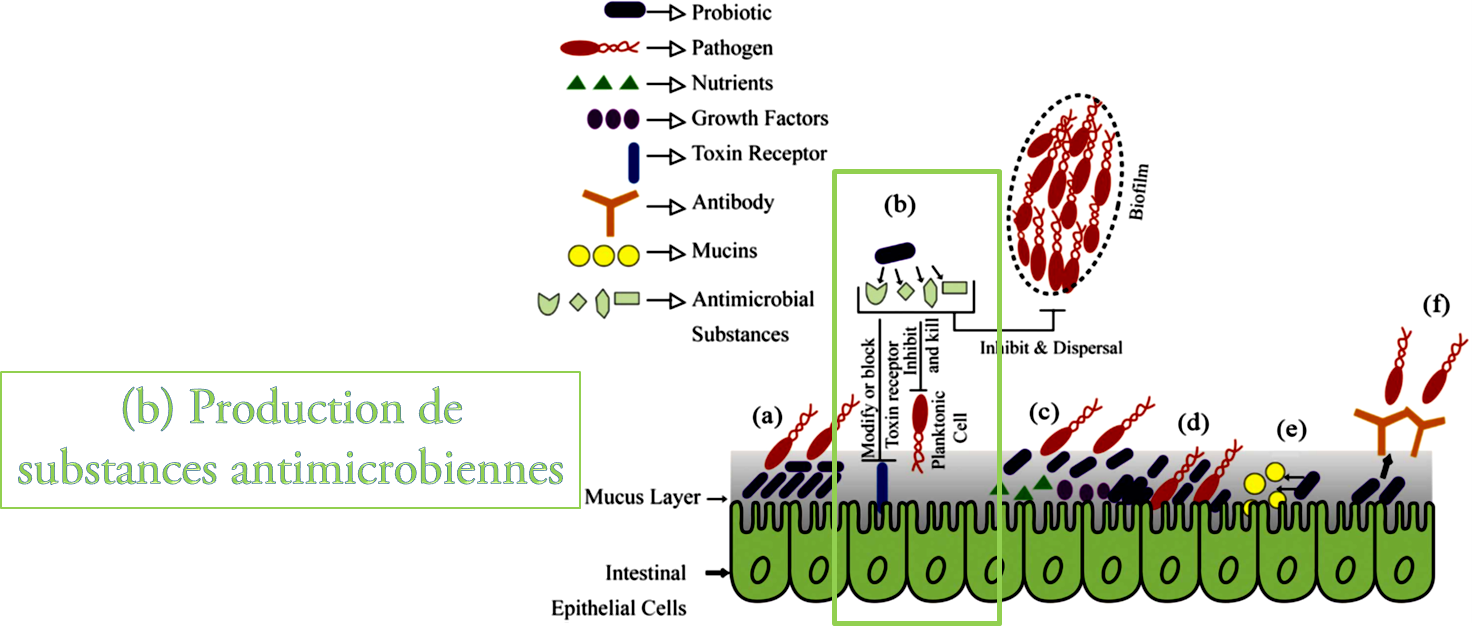
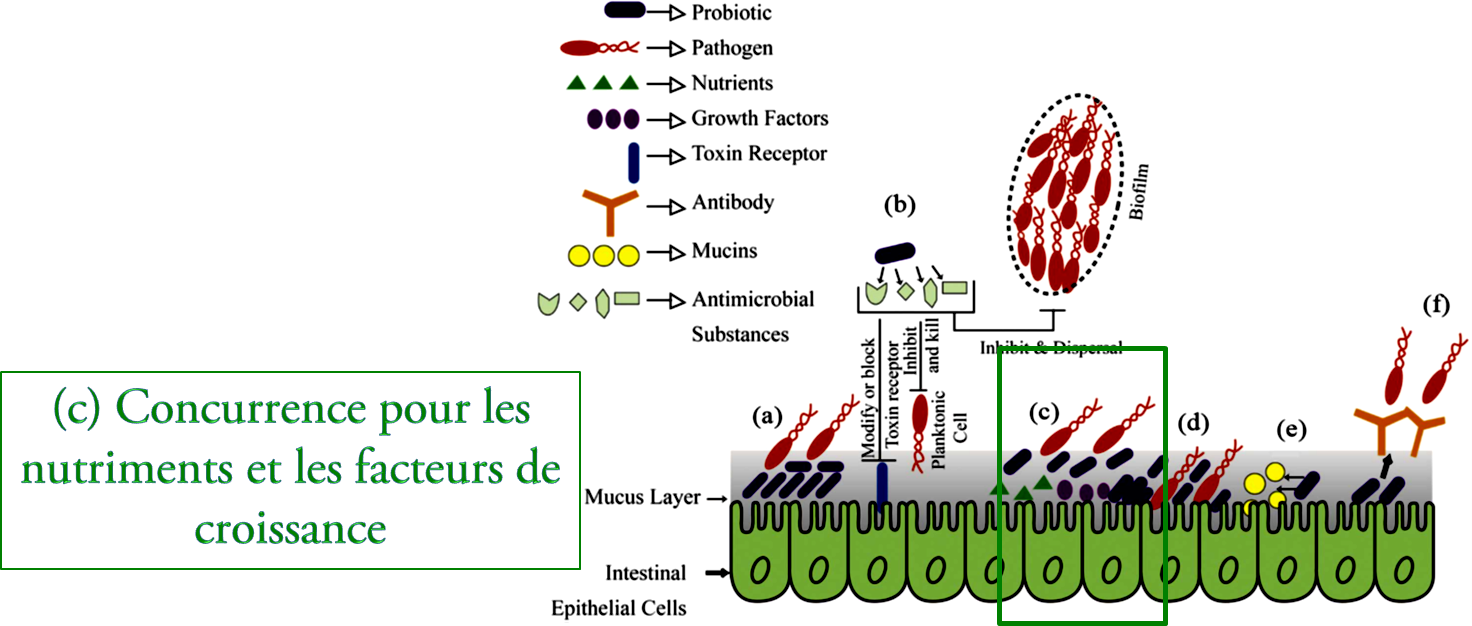
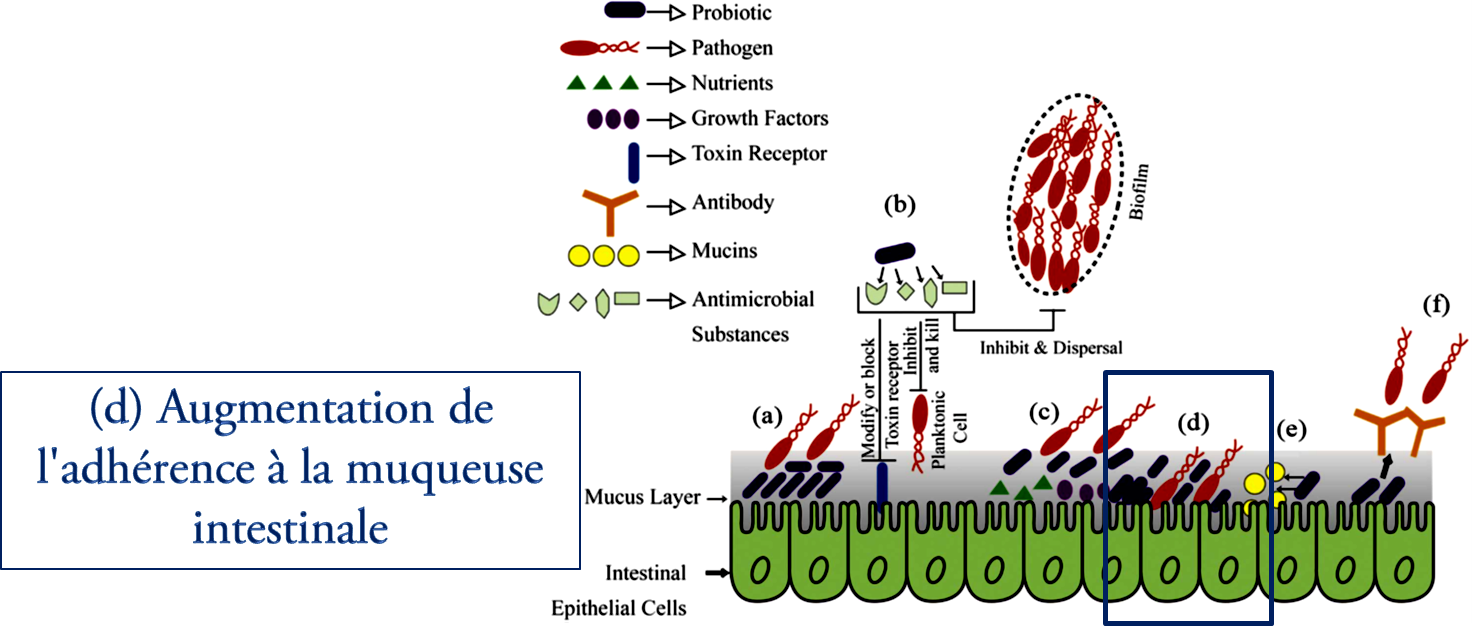
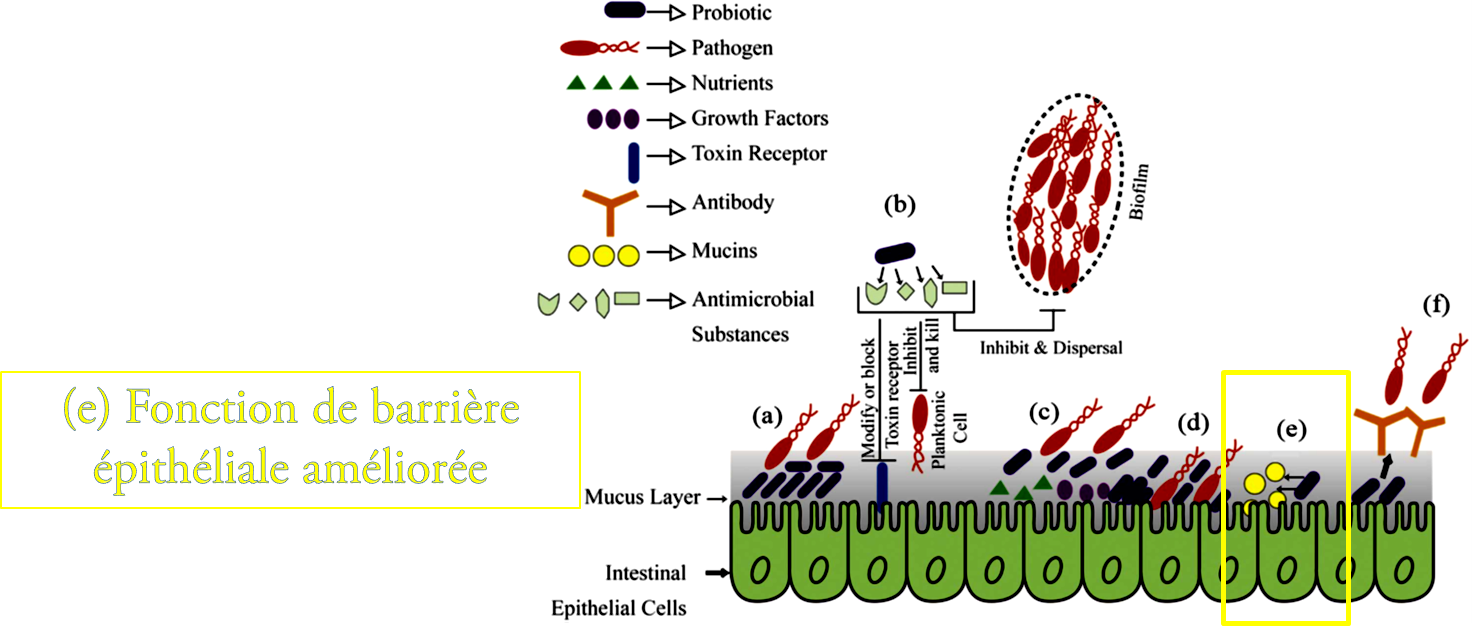
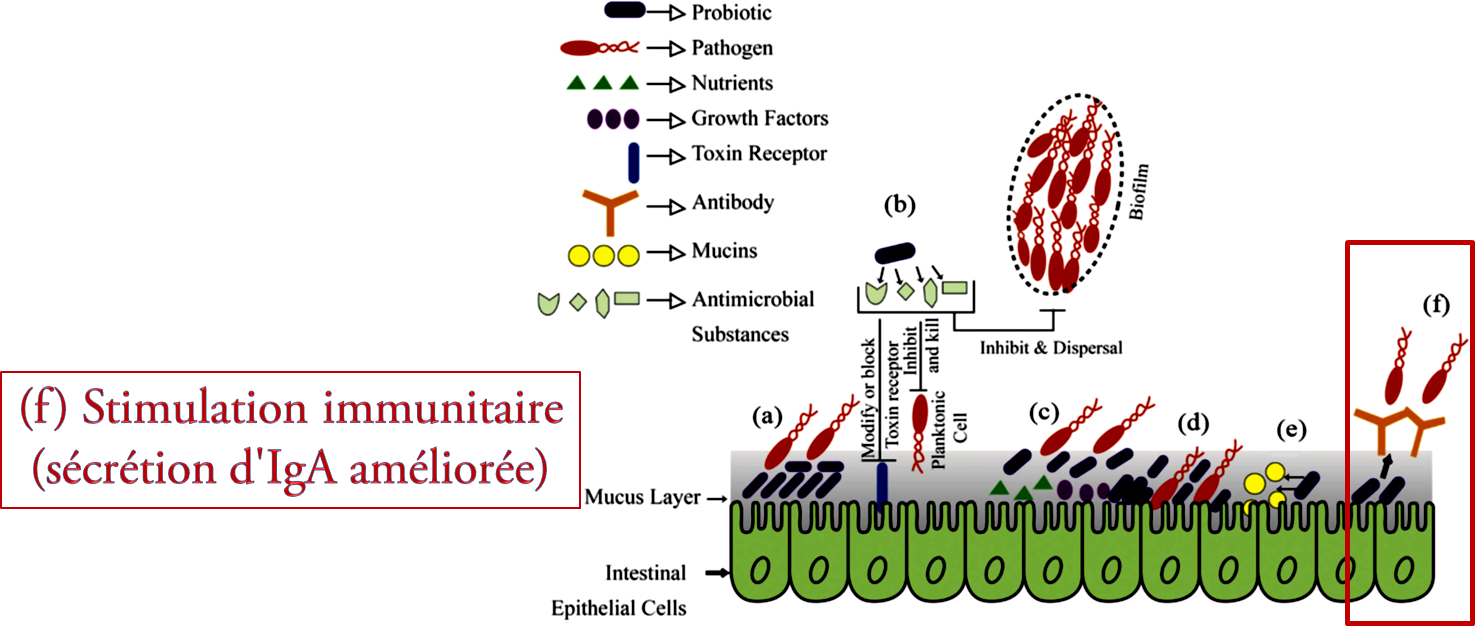
Figure N° 2.1 : Mécanismes d'action des probiotiques à l'intérieur de l'intestin (a), (b), (c), (d) et (F).
Références bibliographiques
Routy B. et al. (2018). Gut microbiome influences efficacy of PD-1-based immunotherapy against epithelial tumors. Science, 359(6371), 91-97. https://doi.org/10.1126/science.aan3706
Plovier H. et al. (2017). A purified membrane protein from Akkermansia muciniphila improves metabolism in obese and diabetic mice. Nature Medicine, 23(1), 107-113. https://doi.org/10.1038/nm.4236
Depommier C. et al. (2019). Supplementation with Akkermansia muciniphila in overweight and obese human volunteers: a proof-of-concept exploratory study. Nature Medicine, 25(7), 1096-1103. https://doi.org/10.1038/s41591-019-0495-2
Dinan T.G. et al. (2019). Psychobiotics and the gut-brain axis: in the pursuit of happiness. Neuropsychiatric Disease and Treatment, 15, 2997-3003.
Zhang M. et al. (2020). Probiotics as adjunct therapy for Helicobacter pylori eradication. Medicine, 99(30), e21210.
Wu Y. et al. (2017). The effect of probiotics on lipid profiles: A systematic review and meta-analysis of randomized controlled trials. Medicine, 96(51), e8850.
Pinto-Sanchez M.I. et al. (2017). Probiotic Bifidobacterium longum NCC3001 reduces depression scores and alters brain activity: A pilot study in patients with irritable bowel syndrome. Gastroenterology, 153(2), 448-459. https://doi.org/10.1053/j.gastro.2017.05.003
Haskard C.A. et al. (2001). Surface binding of aflatoxin B1 by lactic acid bacteria. Applied and Environmental Microbiology, 67(7), 3086-3091. https://doi.org/10.1128/AEM.67.7.3086-3091.2001
-
République Algérienne Démocratique et Populaire
Ministère de l'Enseignement Supérieur et de la Recherche Scientifique
Centre Universitaire Nour Bachir – El-Bayadh
Département des Sciences Biologiques
Microorganismes Thérapeutiques
Master 2 – Microbiologie Appliquée | Semestre II
PARTIE 3 — Applications thérapeutiques
Alimentation, santé animale, phagothérapie, levures/moisissures thérapeutiques & perspectives génomiques
Dr. NAIMI Mostefa
Maître de Conférences A – Département des Sciences Biologiques
Année universitaire 2025–2026
Partie 3 — Applıcatıons thérapeutıques
3.1 Prévention des maladies d'origine alimentaire
3.1.1 Épidémiologie et agents pathogènes d'origine alimentaire
Les maladies d'origine alimentaire, ou type alimentaire, constituent un problème de santé publique mondial majeur. L'OMS estime à 600 millions le nombre de cas et 420 000 décès annuels dans le monde. En Algérie, les TIAC (Toxi-Infections Alimentaires Collectives) demeurent un problème significatif avec un contexte climatique favorisant la prolifération microbienne.
Agent pathogène
Source alimentaire principale
Mécanisme pathogène
Probiotique préventif
Salmonella spp.
Volailles, œufs, produits laitiers
Invasion entérocytes ; toxines ; réponse inflammatoire
Lacticaseibacillus rhamnosus GG, L. acidophilus
Campylobacter jejuni
Volailles (poulet), eau non traitée
Invasion ; toxines cytoletales (CDT)
Bifidobacterium breve, L. rhamnosus
Listeria monocytogenes
Fromages à pâte molle, charcuteries
Invasion intracellulaire ; listériolysine O
Enterococcus faecium, L. plantarum (biocontrôle alimentaire)
Clostridium perfringens
Viandes cuites refroidies lentement
Toxine alpha (phospholipase C)
Bacillus subtilis (compétition nutritionnelle)
Staphylococcus aureus
Produits laitiers, charcuteries
Entérotoxines préformées thermostables
Lactococcus lactis (compétition, bactériocines nisine)
E. coli entérohémorragique O157:H7
Viande hachée, légumes crus
Toxine de Shiga (Stx1, Stx2) ; lésion A/E
Limosilactobacillus fermentum, L. rhamnosus GG
3.1.2 Mécanismes de protection par les probiotiques
• Exclusion compétitive sur la muqueuse digestive : colonisation préventive des sites de liaison des pathogènes (récepteurs de Lewis b, fibronectine, collagène)
• Production de substances antimicrobiennes :
– Nisine (Lactococcus lactis) : bactériocine de classe I active contre les bactéries Gram+ sporulantes dont Listeria et Clostridium.
– Acidoline, acidophiline (L. acidophilus) : actives contre E. coli, Salmonella, Shigella.
– Reutérine (Limosilactobacillus reuteri) : large spectre incluant E. coli O157:H7, Salmonella, Campylobacter.
• Immunostimulation préventive : renforcement de la barrière muqueuse et production d'IgA sIgA avant contact avec l'agent pathogène.
• Biocontrôle alimentaire : utilisation des bactéries lactiques dans les aliments fermentés comme barrière microbiologique naturelle (hurdle technology).
3.1.3 Applications dans les aliments fonctionnels — Algérie & Maghreb
Les aliments fermentés traditionnels algériens constituent une source ancestrale de microorganismes probiotiques :
• Lben (لبن) : lait fermenté acide contenant L. bulgaricus, S. thermophilus, L. acidophilus — protection contre les diarrhées estivales.
• Raïb (رائب) : yaourt à caillé ferme — source de Bifidobacterium et Lactobacillaceae
• Jben (جبن) : fromage frais traditionnel — contient des Enterococcus et Lactococcus lactis producteurs de nisine.
• Khli (خليع) : viande séchée fermentée — présence de bactéries lactiques protectrices contre Listeria et Clostridium.
Perspectives de valorisation : standardisation et validation scientifique des souches probiotiques isolées de ces aliments fermentés traditionnels pour mise sur le marché de probiotiques d'origine locale.
3.2 Stimulation de la croissance des animaux
3.2.1 Contexte réglementaire : interdiction des antibiotiques facteurs de croissance
Suite à l'interdiction européenne des antibiotiques comme facteurs de croissance (AFC) dès 2006 (Règlement CE n°1831/2003), puis à l'élargissement de cette politique au niveau mondial (OMS, Plan d'Action Mondial sur la Résistance aux Antimicrobiens, 2015–2020), les probiotiques zootechniques sont devenus une alternative incontournable en production animale.
En Algérie, le décret exécutif n°21-188 (2021) renforce les restrictions sur l'usage des antibiotiques en élevage, ouvrant la voie au développement des probiotiques zootechniques.
3.2.2 Espèces probiotiques utilisées en production animale
Microorganisme
Espèce animale ciblée
Mécanisme d'action principal
Gain de performance
Bacillus subtilis (ex : QST 713)
Volailles (poulet de chair, dinde)
Enzymes digestives (protéases, amylases, xylanases) ; exclusion compétitive Salmonella
Amélioration IC 3–5 % ; réduction mortalité
Bacillus licheniformis
Porcs, volailles
Production de bacitracine naturelle ; amélioration digestibilité protéines
Gain poids vif +4–8 %
Lacticaseibacillus acidophilus + Bifidobacterium animalis
Bovins laitiers
Stabilisation microbiote ruminal ; amélioration digestion fibres ; production lait
Augmentation production lait +3–6 %
Saccharomyces cerevisiae (levure active)
Ruminants (bovins, ovins, caprins)
Consommation O₂ résiduel (anaérobiose ruminale) ; stimulation bactéries cellulolytiques du rumen
Amélioration digestibilité fibre NDF +5–10 %
Enterococcus faecium (NCIMB 11181)
Porcs, volailles
Acidification intestinale ; exclusion compétitive pathogènes (E. coli, Salmonella)
Réduction diarrhées post-sevrage porcins
Lactobacillus acidophilus + L. casei + Bifidobacterium
Aquaculture (saumon, tilapia)
Amélioration immunité innée ; résistance aux infections bactériennes (Aeromonas, Vibrio)
Survie +10–20 % ; poids vif +8 %
3.2.3 Mécanismes zootechniques des probiotiques
• Amélioration de l'intégrité intestinale : augmentation de la hauteur des villosités intestinales et de la profondeur des cryptes → augmentation de la surface d'absorption.
• Optimisation de la digestibilité : production d'enzymes digestives complémentaires (phytases, xylanases, protéases) → meilleure valorisation des aliments.
• Amélioration de la microflore ruminale (ruminants) : stabilisation du pH ruminal, stimulation des bactéries cellulolytiques (Ruminococcus, Fibrobacter succinogenes).
• Réduction de l'excrétion de pathogènes : diminution de Salmonella, Campylobacter dans les fientes de volailles → sécurité des produits alimentaires d'origine animale.
• Amélioration de la qualité des produits : teneur en AGPI (acides gras polyinsaturés) et en antioxydants dans les œufs et la viande.
3.3 Phagothérapie — Principes fondamentaux et applications cliniques
La phagothérapie (ou virothérapie bactérienne) est l'utilisation thérapeutique de bactériophages (virus des bactéries) pour traiter des infections bactériennes. Abandonnée en Occident avec l'avènement des antibiotiques dans les années 1940, elle connaît un regain d'intérêt majeur dans le contexte de la résistance antimicrobienne (RAM) mondiale.
3.3.1 Biologie des bactériophages — Rappels essentiels
Caractéristiques essentielles des phages thérapeutiques
• Spécificité d'hôte : chaque phage infecte spécifiquement une ou quelques souches bactériennes (tropisme étroit) → précision thérapeutique sans perturbation du microbiote commensale
• Cycle lytique (obligatoire pour usage thérapeutique) : adsorption → injection ADN → réplication → lyse bactérienne → libération de nouveaux phages (burst size : 50–200 phages/bactérie)
• Cycle lysogène (à éviter absolument en thérapeutique) : intégration dans le chromosome bactérien → transfert possible de gènes de virulence (transduction spécialisée) → contre-indication pour usage médical
• Auto-amplification in situ : les phages se multiplient au site d'infection tant que des bactéries cibles sont présentes → effet dose-dépendant auto-entretenu
• Inoffensifs pour les cellules eucaryotes : absence de récepteurs bactériens sur les cellules humaines
3.3.2 Classification des phages d'intérêt thérapeutique (ICTV 2022)
Famille / Ordre
Morphologie
Type d'acide nucléique
Exemples thérapeutiques
Caudoviricetes (ordre Caudovirales)
Queue (myovirus, siphovirus, podovirus)
ADN double brin
Phages anti-Pseudomonas, anti-Staphylococcus
Myoviridae
Queue contractile (ex : T4, Mu)
ADN db
Anti-E. coli, anti-Klebsiella
Siphoviridae
Queue non contractile longue (ex : λ)
ADN db
Anti-Mycobacterium (PhAlerT)
Podoviridae
Queue courte (ex : T7, P22)
ADN db
Anti-Salmonella, anti-E. coli
Inoviridae
Filamenteux
ADN simple brin
Phages filamenteux (moins utilisés)
Microviridae
Icosaédrique sans queue
ADN sb circulaire
PhiX174 (modèle expérimental)
3.3.3 Phagothérapie clinique
La phagothérapie a connu des avancées cliniques majeures dans les années 2020, principalement portées par la crise de la résistance antimicrobienne (RAMm) et les infections à bactéries multirésistantes (BMR).
Cas clinique emblématique — Première utilisation intraveineuse approuvée (FDA, 2016)
Patient : Tom Patterson (UCSD), infection à Acinetobacter baumannii multirésistante (pandrug-resistant) après un séjour en Égypte. État critique : coma septique.
Traitement : Autorisation compassionnelle FDA → administration IV de phages purifiés (2 cocktails : phages de l'Institut Eliava de Tbilissi + phages Navy/USNAMRU).
Résultat : éradication complète de l'infection en 6 semaines, récupération neurologique totale.
Référence : Schooley et al. (2017).
Essais cliniques en cours (2022–2026)
Indication
Phase
Phages ciblant
Centre / Pays
Infections pulmonaires à P. aeruginosa (mucoviscidose)
Phase II
Pseudomonas aeruginosa (cocktail PHAGOBIOTICS)
CHU Paris-Sorbonne / France
Infections sur matériel prothétique (ostéite)
Phase II
S. aureus, S. epidermidis
PHAGOTHERAPY Trial — Belgique, France
Infections urinaires récidivantes
Phase II
E. coli uropathogène
PhagoBurn II — Europe
Infections à Klebsiella pneumoniae KPC
Phase I/II compassionnel
Klebsiella pneumoniae MDR
Multiple centres USA (PHAGE Trial)
Maladie de Crohn (E. coli adhérent-invasif)
Phase II
E. coli AIEC (adherent-invasive)
Université de Birmingham / Royaume-Uni
3.3.4 Avantages et limites de la phagothérapie
Avantages par rapport aux antibiotiques
• Spécificité d'hôte : inactivité vis-à-vis du microbiote commensale (absence de dysbiose iatrogène)
• Auto-amplification au site d'infection : doses plus faibles requises
• Efficacité contre les bactéries multirésistantes (BMR) : mécanismes de résistance aux antibiotiques sans effet sur la sensibilité aux phages
• Biofilm : les phages produisent des dépolymérases spécifiques dégradant la matrice exopolysaccharidique des biofilms
• Évolution rapide : possibilité de sélectionner de nouveaux phages en réponse à l'émergence de mutants résistants
Limites et défis
• Résistance bactérienne aux phages : modification des récepteurs de surface, production de protéines anti-phages (anti-CRISPR), superinfection exclusion
• Neutralisation par le système immunitaire : anticorps anti-phages neutralisants après administration répétée
• Spectre étroit : nécessite l'identification préalable de la souche bactérienne (phagogramme) → délai de traitement
• Réglementation : statut réglementaire ambigu (médicament, préparation magistrale ou dispositif médical) → frein au développement commercial
• Production et contrôle qualité : purification des phages (élimination des endotoxines bactériennes) ; stabilité des préparations
• Transfert de gènes de résistance : risque avec les phages lysogènes → sélection stricte de phages lytiques obligatoires
3.4 Levures et moisissures à usage thérapeutique
Au-delà des bactéries probiotiques classiques, les levures et moisissures offrent un potentiel thérapeutique considérable, tant comme microorganismes probiotiques directs que comme producteurs de métabolites bioactifs.
3.4.1 Levures thérapeutiques
Saccharomyces cerevisiae var. boulardii — le probiotique levurien de référence
Statut : seule levure dont le statut probiotique est formellement reconnu par les sociétés savantes (ESPGHAN, WGO). Résistante à tous les antibiotiques (eucaryote) — avantage majeur lors des traitements antibiotiques.
Mécanismes d'action :
• Production de protéases neutralisant les toxines A et B de Clostridioides difficile.
• Production d'une phosphatase neutralisant l'endotoxine (LPS) d'E. coli.
• Stimulation de la production d'IgA sIgA et de polyamines (spermine, spermidine) trophiques pour la muqueuse.
• Exclusion compétitive de Candida albicans et de C. difficile.
Indications validées (méta-analyses Cochrane) :
• Diarrhée associée aux antibiotiques : réduction du risque de 47 % (Szajewska et al., 2015).
• Infections à Clostridioides difficile : prévention des récidives (RR = 0,59).
• Diarrhée aiguë du nourrisson : réduction de la durée de 24h en moyenne.
• Diarrhée du voyageur : efficacité préventive documentée.
Autres levures à potentiel thérapeutique
Levure
Application thérapeutique
Mécanisme principal
Statut réglementaire
Kluyveromyces marxianus
Intolérance au lactose ; fermentations laitières fonctionnelles
Production β-galactosidase thermostable ; AGCC par fermentation
GRAS (FDA) ; QPS (EFSA)
Kluyveromyces lactis
Intolérance au lactose ; production de β-galactosidase commerciale
Hydrolyse enzymatique du lactose in situ
GRAS (FDA)
Candida albicans (souches avirulentes)
Modulation immunitaire muqueuse — recherche
Stimulation Th17 ; induction tolérance orale (expérimental)
Recherche préclinique uniquement
Pichia kudriavzevii (ex-Candida krusei)
Biocontrôle alimentaire ; fermentations traditionnelles
Compétition avec pathogènes fongiques ; production éthanol
Restriction d'usage (résistance azolés)
Torulaspora delbrueckii
Fermentations œnologiques fonctionnelles ; arômes bioactifs
Production de glutathion ; activité antioxydante
GRAS (usage alimentaire)
3.4.2 Moisissures à usage thérapeutique
Les moisissures (champignons filamenteux) contribuent à la thérapeutique principalement comme producteurs industriels de molécules bioactives, mais aussi directement dans les aliments fermentés thérapeutiques.
• Aspergillus oryzae :
– Production d'enzymes digestives : amylases, protéases, lipases — utilisées dans les compléments enzymatiques digestifs (insuffisance pancréatique exocrine).
– Fermentation du miso, saké, sauce soja — aliments fermentés aux propriétés antioxydantes et prébiotiques documentées.
– Statut GRAS (FDA) pour usage alimentaire.
• Aspergillus niger :
– Production commerciale d'acide citrique (utilisé comme antioxydant, agent chélatant, acidifiant pharmaceutique).
– Production de glucoamylases industrielles pour production de sirops de glucose.
• Penicillium camemberti / Penicillium roquefortii :
– Fermentations fromagères thérapeutiques : production de peptides bioactifs (antihypertenseurs, anticancéreux) libérés par protéolyse de la caséine.
– Probiotiques alimentaires traditionnels dans les fromages à croûte fleurie et persillés.
• Rhizopus oligosporus (tempeh indonésien) :
– Production d'isoflavones de soja aglycones (génistéine, daidzéine) par biotransformation — activité phyto-œstrogène, anticancéreuse.
– Production de vitamine B12 (cas rare pour un champignon) et de protéines complètes.
3.4.3 Champignons médicinaux (Nutraceutiques)
Espèce
Composés bioactifs
Activités thérapeutiques documentées
Ganoderma lucidum (Reishi)
Polysaccharides (bêta-glucanes), triterpènes (acides ganodériques)
Immunomodulation, activité anti-tumorale, hépatoprotection, adaptogène
Lentinus edodes (Shiitaké)
Lentinane (bêta-1,3-glucane)
Immunostimulation, activité anti-VIH documentée, anti-tumorale (adjuvant oncologie au Japon)
Trametes versicolor (Queue de Dindon)
PSK (polysaccharide-K = Krestin), PSP
Immunostimulant anti-tumoral approuvé au Japon (cancer colorectal, gastrique, pulmonaire)
Hericium erinaceus (Lion's Mane)
Héricénones, érinacines (stimulants NGF)
Neurostimulation (Nerve Growth Factor), prévention maladies neurodégénératives, mémoire
Cordyceps sinensis / militaris
Cordycépine (3'-déoxyadenosine), adénosine
Amélioration VO2max, anti-fatigue, immunomodulation, propriétés antivirales
3.5 Amélioration génétique des souches probiotiques et perspectives
3.5.1 Approches classiques d'amélioration
L'optimisation des propriétés probiotiques par des approches génétiques vise à amplifier les caractéristiques fonctionnelles naturelles des souches ou à leur conférer de nouvelles capacités thérapeutiques.
• Mutagenèse aléatoire (UV, NTG) suivie de sélection phénotypique : amélioration de la résistance au pH acide, à la bile, à la chaleur (lyophilisation).
• Adaptation évolutive (adaptive laboratory evolution, ALE) : passages répétés dans des conditions de stress → sélection de mutants spontanés présentant des caractéristiques améliorées.
• Sélection sur critères fonctionnels : criblage à haut débit (microfluidique, cytométrie en flux) pour identifier les souches à adhésion améliorée.
• Hybridation naturelle entre souches (conjugaison, transformation) : transfert de plasmides portant des gènes bénéfiques (bactériocines, enzymes).
3.5.2 Ingénierie génétique des probiotiques — Approches modernes
Les biotechnologies modernes permettent de concevoir des probiotiques « de précision » (designer probiotics) avec des fonctions thérapeutiques spécifiques :
Probiotiques de précision — Exemples documentés
• Lacticaseibacillus rhamnosus GG modifié pour la production de GLP-1 (glucagon-like peptide-1) : traitement adjuvant du diabète de type 2 (études précliniques)
• E. coli Nissle 1917 engineered : expression d'anticorps à fragment simple chaîne (scFv) neutralisant les toxines d'entéropathogènes (Shiga toxine) — usage intestinal (études phase I)
• E. coli Nissle 1917 - SYNB1891 : production de cytokines immunostimulatrices intra-tumorales (STING agoniste) pour usage en oncologie (NCT04167137, Phase I)
• Bifidobacterium longum exprimant de l'IL-10 : réduction de l'inflammation dans les MICI — essais précliniques prometteurs
• L. lactis produisant de l'IL-10 humaine (première application de phytothérapie génique muqueuse — Steidler et al., 2000) : preuve de concept fondatrice
3.5.3 CRISPR-Cas9 et édition du microbiome
L'outil CRISPR-Cas9 révolutionne l'ingénierie des probiotiques et ouvre de nouvelles perspectives :
• Édition précise du génome des souches probiotiques : introduction de gènes thérapeutiques, suppression de facteurs de virulence résiduels, modification du tropisme d'hôte..
• CRISPR antimicrobien (CRISPR-Cas9 vectorisé par phages) : destruction ciblée de gènes de résistance aux antibiotiques dans les bactéries pathogènes — alternative aux antibiotiques.
• Contrôle du microbiome : sélection in vivo de souches spécifiques du microbiome pour modifier sa composition vers un profil bénéfique (microbiome editing).
• Kill switch génétique : intégration de systèmes de contrôle (auxotrophies, commutateurs génétiques inductibles) pour confiner les probiotiques engineerés dans l'intestin → biosécurité.
3.5.4 Cadre réglementaire des probiotiques OGM
L'ingénierie génétique des probiotiques soulève des questions réglementaires et éthiques importantes :
• Union européenne : les probiotiques OGM sont soumis au Règlement (CE) n°1829/2003 (OGM alimentaires) et au Règlement (CE) n°1946/2003 (mouvements transfrontières OGM) → autorisation stricte cas par cas.
• États-Unis : procédure FDA de LBP (Live Biotherapeutic Products) = cadre réglementaire spécifique.
• Algérie : Loi n°00-11 relative aux semences et plants (transposable aux microorganismes OGM) ; arrêté ministériel en cours d'élaboration sur les LBP.
• Principe de précaution : évaluation obligatoire de la dissémination environnementale, des transferts de gènes horizontaux et des effets sur le microbiome résidant
3.5.5 Perspectives — Microbiome thérapeutique 2030
Tendances majeures 2025–2030
• Médecine de précision microbiomique : sélection du probiotique en fonction du profil métagénomique individuel du patient
• Consortia microbiens définis (SER-109, Vowst® — premier médicament microbiote approuvé FDA 2023) : assemblages de spores de Firmicutes pour traitement de Clostridioides difficile récurrent
• Transplantation de microbiote fécal (TMF) standardisée : développement de banques de microbiotes certifiés (Rebiotix, Vedanta)
• Postbiotiques de précision : utilisation de métabolites purifiés (butyrate encapsulé, urolithines, équol) contournant les contraintes de viabilité des probiotiques
• Bioimprimerie 3D de microorganismes thérapeutiques : encapsulation dans des matrices alginate/chitosan pour libération ciblée colique
• Intelligence artificielle et microbiome : prédiction des dysbioses par machine learning ; sélection algorithmique des consortia probiotiques optimaux
Références bibliographiques
Schooley R.T. et al. (2017). Development and Use of Personalized Bacteriophage-Based Therapeutic Cocktails To Treat a Patient with a Disseminated Resistant Acinetobacter baumannii Infection. Antimicrobial Agents and Chemotherapy, 61(10), e00954-17. https://doi.org/10.1128/AAC.00954-17
Dedrick R.M. et al. (2019). Engineered bacteriophages for treatment of a patient with a disseminated drug-resistant Mycobacterium abscessus. Nature Medicine, 25(5), 730-733. https://doi.org/10.1038/s41591-019-0437-z
Szajewska H. et al. (2015). Saccharomyces boulardii CNCM I-745 in the prevention of antibiotic-associated diarrhoea in children: a randomized double-blind placebo-controlled trial. Journal of Pediatrics, 166(2), 414-420.
Steidler L. et al. (2000). Treatment of murine colitis by Lactococcus lactis secreting interleukin-10. Science, 289(5483), 1352-1355. https://doi.org/10.1126/science.289.5483.1352
Riglar D.T. & Silver P.A. (2018). Engineering bacteria for diagnostic and therapeutic applications. Nature Reviews Microbiology, 16(4), 214-225. https://doi.org/10.1038/nrmicro.2017.172
Zheng D. et al. (2020). Interaction between microbiota and immunity in health and disease. Cell Research, 30(6), 492-506. https://doi.org/10.1038/s41422-020-0332-7
OMS (2019). Nouveau rapport : La résistance aux antibiotiques met en péril les progrès en médecine. Rapport mondial sur la surveillance de la résistance aux antimicrobiens 2019.
Barrangou R. & Doudna J.A. (2016). Applications of CRISPR technologies in research and beyond. Nature Biotechnology, 34(9), 933-941. https://doi.org/10.1038/nbt.3659
FDA (2023). Vowst (fecal microbiota spores, live-brpk) - First FDA-approved fecal microbiota product. FDA News Release, April 2023.
Torres-Barceló C. (2018). The disparate effects of bacteriophages on antibiotic-resistant bacteria. Emerging Microbes & Infections, 7(1), 1-12. https://doi.org/10.1038/s41426-018-0169-z
-
-
Cryan J.F. et al. (2019). The Microbiota-Gut-Brain Axis. Physiological Reviews, 99(4), 1877–2013. https://doi.org/10.1152/physrev.00018.2018
Gibson G.R. et al. (2017). Expert consensus document: The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of prebiotics. Nature Reviews Gastroenterology & Hepatology, 14(8), 491–502. https://doi.org/10.1038/nrgastro.2017.75
Hill C. et al. (2014). Expert consensus document. The International Scientific Association for Probiotics and Prebiotics consensus statement on the scope and appropriate use of the term probiotic. Nature Reviews Microbiology, 12(8), 506–514. https://doi.org/10.1038/nrgastro.2014.66
Journal Officiel de la République Algérienne — Décret exécutif n° 23-106 relatif aux compléments alimentaires : dispositions applicables aux produits contenant des microorganismes vivants.
Routy B. et al. (2018). Gut microbiome influences efficacy of PD-1-based immunotherapy against epithelial tumors. Science, 359(6371), 91-97. https://doi.org/10.1126/science.aan3706
Plovier H. et al. (2017). A purified membrane protein from Akkermansia muciniphila improves metabolism in obese and diabetic mice. Nature Medicine, 23(1), 107-113. https://doi.org/10.1038/nm.4236
Depommier C. et al. (2019). Supplementation with Akkermansia muciniphila in overweight and obese human volunteers: a proof-of-concept exploratory study. Nature Medicine, 25(7), 1096-1103. https://doi.org/10.1038/s41591-019-0495-2
Dinan T.G. et al. (2019). Psychobiotics and the gut-brain axis: in the pursuit of happiness. Neuropsychiatric Disease and Treatment, 15, 2997-3003.
Zhang M. et al. (2020). Probiotics as adjunct therapy for Helicobacter pylori eradication. Medicine, 99(30), e21210.
Wu Y. et al. (2017). The effect of probiotics on lipid profiles: A systematic review and meta-analysis of randomized controlled trials. Medicine, 96(51), e8850.
Pinto-Sanchez M.I. et al. (2017). Probiotic Bifidobacterium longum NCC3001 reduces depression scores and alters brain activity: A pilot study in patients with irritable bowel syndrome. Gastroenterology, 153(2), 448-459. https://doi.org/10.1053/j.gastro.2017.05.003
Haskard C.A. et al. (2001). Surface binding of aflatoxin B1 by lactic acid bacteria. Applied and Environmental Microbiology, 67(7), 3086-3091. https://doi.org/10.1128/AEM.67.7.3086-3091.2001
Lopez-Siles M. et al. (2017). Faecalibacterium prausnitzii: from microbiology to diagnostics and prognostics. ISME Journal, 11(4), 841–852. https://doi.org/10.1038/ismej.2016.176
Plovier H. et al. (2017). A purified membrane protein from Akkermansia muciniphila or the pasteurized bacterium improves metabolism in obese and diabetic mice. Nature Medicine, 23(1), 107-113. https://doi.org/10.1038/nm.4236
Salminen S. et al. (2021). The International Scientific Association of Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of postbiotics. Nature Reviews Gastroenterology & Hepatology, 18(9), 649-667. https://doi.org/10.1038/s41575-021-00440-6
Shreiner A.B. et al. (2015). The gut microbiome in health and in disease. Current Opinion in Gastroenterology, 31(1), 69-75. https://doi.org/10.1097/MOG.0000000000000139
Swanson K.S. et al. (2020). The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of synbiotics. Nature Reviews Gastroenterology & Hepatology, 17(11), 687-701. https://doi.org/10.1038/s41575-020-0344-2
Wastyk H.C. et al. (2021). Gut-microbiota-targeted diets modulate human immune status. Cell, 184(16), 4137-4153. https://doi.org/10.1016/j.cell.2021.06.019*
Zheng J. et al. (2020). A taxonomic note on the genus Lactobacillus: Description of 23 novel genera, emended description of the genus Lactobacillus Beijerinck 1901, and union of Lactobacillaceae and Leuconostocaceae. International Journal of Systematic and Evolutionary Microbiology, 70(4), 2782-2858. https://doi.org/10.1099/ijsem.0.004107
Schooley R.T. et al. (2017). Development and Use of Personalized Bacteriophage-Based Therapeutic Cocktails To Treat a Patient with a Disseminated Resistant Acinetobacter baumannii Infection. Antimicrobial Agents and Chemotherapy, 61(10), e00954-17. https://doi.org/10.1128/AAC.00954-17
Dedrick R.M. et al. (2019). Engineered bacteriophages for treatment of a patient with a disseminated drug-resistant Mycobacterium abscessus. Nature Medicine, 25(5), 730-733. https://doi.org/10.1038/s41591-019-0437-z
Szajewska H. et al. (2015). Saccharomyces boulardii CNCM I-745 in the prevention of antibiotic-associated diarrhoea in children: a randomized double-blind placebo-controlled trial. Journal of Pediatrics, 166(2), 414-420.
Steidler L. et al. (2000). Treatment of murine colitis by Lactococcus lactis secreting interleukin-10. Science, 289(5483), 1352-1355. https://doi.org/10.1126/science.289.5483.1352
Riglar D.T. & Silver P.A. (2018). Engineering bacteria for diagnostic and therapeutic applications. Nature Reviews Microbiology, 16(4), 214-225. https://doi.org/10.1038/nrmicro.2017.172
Zheng D. et al. (2020). Interaction between microbiota and immunity in health and disease. Cell Research, 30(6), 492-506. https://doi.org/10.1038/s41422-020-0332-7
OMS (2019). Nouveau rapport : La résistance aux antibiotiques met en péril les progrès en médecine. Rapport mondial sur la surveillance de la résistance aux antimicrobiens 2019.
Barrangou R. & Doudna J.A. (2016). Applications of CRISPR technologies in research and beyond. Nature Biotechnology, 34(9), 933-941. https://doi.org/10.1038/nbt.3659
FDA (2023). Vowst (fecal microbiota spores, live-brpk) - First FDA-approved fecal microbiota product. FDA News Release, April 2023.
Torres-Barceló C. (2018). The disparate effects of bacteriophages on antibiotic-resistant bacteria. Emerging Microbes & Infections, 7(1), 1-12. https://doi.org/10.1038/s41426-018-0169-z
